Ingredientes ativos: Filgrastim
Nivestim 12 MU / 0,2 ml solução injetável / para perfusão
Nivestim 30 MU / 0,5 ml solução injetável / para perfusão
Nivestim 48 MU / 0,5 ml solução injetável / para perfusão
Por que o Nivestim é usado? Para que serve?
O que é Nivestim
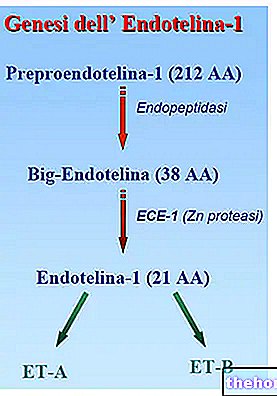
Nivestim contém a substância ativa filgrastim que pertence a um grupo de proteínas chamadas citocinas e é muito semelhante a uma proteína natural (fator estimulador de colônias de granulócitos [G-CSF]) produzida pelo corpo humano. Filgrastim estimula a medula óssea (o tecido que produz novas células sanguíneas) para produzir mais células sanguíneas, especialmente alguns tipos de células brancas do sangue. As células brancas do sangue são importantes porque ajudam o corpo a combater infecções.
Para que é usado o Nivestim
O seu médico receitou-lhe Nivestim para ajudar o seu corpo a produzir mais glóbulos brancos. O seu médico irá explicar porque lhe foi prescrito o Nivestim. Nivestim é útil em uma série de condições clínicas diferentes, tais como:
- quimioterapia
- transplante de medula óssea,
- neutropenia crônica grave (neutropenia é um número anormal baixo de um certo tipo de glóbulo branco também conhecido como neutrófilos),
- neutropenia em pacientes com infecção por HIV,
- mobilização de células-tronco do sangue periférico.
Contra-indicações Quando o Nivestim não deve ser usado
Não use Nivestim
- se tem alergia ao filgrastim ou a qualquer outro componente deste medicamento.
Precauções de uso O que você precisa saber antes de tomar Nivestim
Fale com o seu médico, farmacêutico ou enfermeiro antes de tomar Nivestim: - se tiver qualquer outra doença (especialmente se pensa que tem uma "infecção),
- se tem tosse, febre e dificuldade em respirar. Eles podem ser secundários a problemas pulmonares (consulte também a seção 4 "EVENTOS ADVERSOS POSSÍVEIS"),
- se tiver anemia falciforme (uma doença hereditária do sangue que afeta os glóbulos vermelhos),
- se tem dor abdominal na parte superior esquerda ou se tem dor no ombro. Pode ser uma consequência de uma doença do baço (ver seção 4 "POSSÍVEIS EVENTOS ADVERSOS"),
- se você sofre de doenças específicas do sangue (por exemplo, síndrome de Kostmann, síndrome mielodisplásica, diferentes tipos de leucemia),
- se sofre de osteoporose. O seu médico pode verificar a densidade dos seus ossos regularmente.
Se necessitar de uma cintilografia óssea, informe o seu médico ou enfermeiro que está a ser tratado com Nivestim.
Informe imediatamente o seu médico ou enfermeiro se sentir sinais repentinos de alergia, como erupção cutânea, comichão ou urticária na pele, inchaço da face, lábios, língua ou outras partes do corpo, falta de ar, respiração ruidosa ou dificuldade em respirar durante o tratamento com Nivestim porque estes podem ser sinais de uma reação alérgica grave.
Enquanto estiver a ser tratado com Nivestim, pode necessitar de análises sanguíneas regulares para verificar o número de neutrófilos e outros glóbulos brancos no seu sangue. Com esses dados, o médico determina a eficácia do tratamento e se deve continuar.
Perda de resposta ao filgrastim
Se você diminuiu a resposta ou não manteve a resposta ao tratamento com filgrastim, seu médico investigará as razões, incluindo a possibilidade de você ter desenvolvido anticorpos que neutralizam a atividade do filgrastim.
Interações Quais medicamentos ou alimentos podem alterar o efeito do Nivestim
Não deve ser tratado com Nivestim nas 24 horas antes e 24 horas após o tratamento com quimioterapia.
Informe o seu médico ou farmacêutico se estiver a tomar ou tiver tomado recentemente, ou se vier a tomar outros medicamentos.
Avisos É importante saber que:
Gravidez e amamentação
Consulte o seu médico ou farmacêutico antes de tomar qualquer medicamento.
Filgrastim não foi estudado em mulheres grávidas. É importante que informe o seu médico se estiver grávida, se pensa que pode estar grávida ou se planeia engravidar, pois o seu médico pode decidir que não pode utilizar este medicamento. Filgrastim pode ter efeitos adversos na sua capacidade de engravidar ou levar ao fim da gravidez.
Não se sabe se o filgrastim passa para o leite materno. Portanto, o seu médico pode decidir que você não pode usar este medicamento se estiver amamentando.
Condução e utilização de máquinas
Filgrastim tem efeitos modestos na capacidade de conduzir e utilizar máquinas.Se se sentir cansado, deve ter cuidado ao conduzir ou utilizar máquinas.
Nivestim contém sorbitol
Este medicamento contém sorbitol (E420). Se foi informado pelo seu médico que tem intolerância a alguns açúcares (frutose), contacte-o antes de tomar este medicamento. Este medicamento também contém sódio em menos de 1 mmol (23 mg) por dose e, portanto, é praticamente "isento de sódio".
Dose, Método e Tempo de Administração Como usar o Nivestim: Posologia
Use este medicamento sempre de acordo com as indicações do seu médico. Verifique com seu médico se você não tiver certeza.
Este medicamento é administrado por injeção, por perfusão intravenosa (gota a gota) ou por via subcutânea no tecido localizado diretamente sob a pele.
Se estiver a utilizar este medicamento por injeção subcutânea, o seu médico pode considerar apropriado injetá-lo a si próprio. O seu médico ou enfermeiro mostrar-lhe-á como injectar (as instruções sobre a auto-injecção encontram-se no final deste folheto). Não tente injectar-se a si próprio a menos que tenha recebido formação para o fazer. Algumas informações de que necessita encontram-se no final da página deste folheto, no entanto, para o tratamento adequado da sua doença, é necessária uma cooperação cuidadosa e constante com o seu médico.
A quantidade de Nivestim de que necessita depende da doença para a qual está a tomar Nivestim e do seu peso corporal.
Nivestim e neutropenia associada à quimioterapia
A dose usual em adultos e crianças é de 0,5 milhões de unidades (5 microgramas) por quilograma de peso corporal por dia. Por exemplo, se você pesa 60 kg, sua dose diária é de 30 milhões de unidades (300 microgramas). O tratamento pode durar até 14 dias. Para algumas doenças, pode ser necessário um tratamento prolongado por até cerca de um mês.
Nivestim e transplante de medula óssea
A dose inicial usual é de 1 milhão de unidades (10 microgramas) por quilograma de peso corporal por dia por perfusão. Por exemplo, se você pesa 60 kg, a sua dose diária é de 60 milhões de unidades (600 microgramas). Geralmente, você receberá a primeira dose pelo menos 24 horas após a quimioterapia, mas dentro de 24 horas após um transplante de medula óssea. O médico irá então realizar análises ao sangue para verificar o efeito do tratamento e estabelecer a sua duração.
Nivestim e neutropenia crônica grave
A dose inicial habitual é entre 0,5 milhões (5 microgramas) e 1,2 milhões (12 microgramas) de unidades por quilograma de peso corporal por dia, em dose única ou em dose dividida. O seu médico irá então realizar análises ao sangue para verificar o efeito do tratamento e determinar a dose mais adequada para si.Em caso de neutropenia, é necessário um tratamento prolongado com Nivestim.
Nivestim e neutropenia em pacientes com infecção por HIV
A dose inicial usual é entre 0,1 (1 micrograma) e 0,4 milhões de unidades (4 microgramas) por quilograma de peso corporal por dia. O seu médico irá realizar análises ao sangue em intervalos regulares para verificar o efeito do tratamento. Assim que a contagem dos glóbulos brancos voltar ao normal, a frequência da dosagem pode ser reduzida para menos de uma vez por dia. Manter contagens normais dos glóbulos brancos pode requerem tratamento prolongado com Nivestim.
Nivestim e transplante de células-tronco de sangue periférico
Se está a doar células estaminais para si próprio, a dose habitual é de 0,5 milhões (5 microgramas) a 1 milhão de unidades (10 microgramas) por quilograma de peso corporal por dia. O tratamento com Nivestim dura até 2 semanas. O médico fará exames de sangue para determinar a melhor época para coletar as células-tronco.
Se doar células estaminais para outra pessoa, a dose habitual é de 1 milhão de unidades por quilograma de peso corporal por dia.O tratamento com Nivestim dura 4 a 5 dias.
Se você esquecer de usar o Nivestim
Caso se tenha esquecido de injetar uma dose, contacte o seu médico ou farmacêutico e pergunte-lhes quando deve injetar a próxima dose. Não use uma dose a dobrar para compensar uma injeção que se esqueceu.
Como termina o tratamento com Nivestim
O seu médico irá informá-lo quando deve parar de utilizar o Nivestim. É normal ter vários cursos de tratamento com Nivestim.
Caso ainda tenha dúvidas sobre a utilização do medicamento, fale com o seu médico ou farmacêutico.
Superdosagem O que fazer se você tiver tomado Nivestim em demasia
Se utilizar mais Nivestim do que deveria, contacte o seu médico ou farmacêutico assim que possível.
Efeitos colaterais Quais são os efeitos colaterais do Nivestim
Como todos os medicamentos, este medicamento pode causar efeitos colaterais, embora nem todas as pessoas os tenham.
Foram notificadas reações de tipo alérgico ao filgrastim, incluindo erupção cutânea, aumento das áreas cutâneas com comichão e anafilaxia (fraqueza, queda da tensão arterial, dificuldade em respirar e engolir e inchaço da face). Se você acha que tem esses tipos de reações, pare de tomar as injeções de Nivestim e procure ajuda médica imediatamente.
Aumento do tamanho do baço e casos muito raros de ruptura do baço foram relatados. Alguns casos de ruptura do baço foram fatais. É importante que contacte o seu médico imediatamente se sentir dor na parte superior esquerda do abdómen ou na omoplata, pois pode ser um sinal de problemas com o baço.
Informe o seu médico imediatamente se você tiver um ou mais dos seguintes eventos adversos durante o tratamento:
- inchaço ou inchaço, que pode estar relacionado à diminuição da micção, dificuldade em respirar, inchaço e sensação de saciedade e uma sensação geral de cansaço. Esses sintomas geralmente aparecem rapidamente.
Estes podem ser sintomas de uma doença pouco frequente (pode afetar até 1 em 100 pessoas) conhecida como "Síndrome do Fuga Capilar", que faz com que o sangue vaze para o corpo a partir de pequenos vasos sanguíneos e que requer atenção médica urgente.
Também é muito importante informar o seu médico se você acha que tem uma "infecção. Há muitas maneiras de uma" infecção se manifestar. Você deve verificar se a temperatura não é e não excede 37,8 ° C, calafrios ou outros sinais de infecção, como vermelhidão da pele, dor de garganta, diarreia, dor de ouvido, dificuldade ou dor ao respirar ou problemas como tosse e asma. Esses sintomas podem ser devido a efeitos adversos pulmonares graves, como pneumonia e síndrome da dificuldade respiratória em adultos, que podem causar a morte. Se tiver febre ou qualquer outro sintoma, contacte o seu médico imediatamente e vá directamente para o hospital.
Se tiver anemia falciforme, certifique-se de que informa o seu médico antes de iniciar o tratamento com Nivestim. Crises de anemia falciforme foram relatadas em alguns pacientes com esta doença tratados com filgrastim.
Eventos adversos muito comuns (afetam mais de 1 em 10 pacientes)
- Sentir-se ou estar doente
- Dor nos ossos e músculos. Pergunte ao seu médico qual medicamento tomar para aliviar este
- Sangramento nasal
- Queda nos níveis de glicose no sangue que pode fazer com que você sinta fome, enjoo, fraqueza, cansaço, tremor ou confusão, ou pode causar sudorese, dores de cabeça, visão turva ou aumento da frequência cardíaca
- Aumento dos valores das enzimas hepáticas ou alterações nas análises ao sangue. Seu médico fará exames de sangue para verificar isso
- Aumento de ácido úrico que pode se manifestar com gota
- Dor no peito
Eventos adversos comuns (afetam até 1 em 10 pacientes)
- Fraqueza
- Fadiga generalizada
- Dor de cabeça
- Constipação ou diarreia
- Perda de apetite
- Inflamação e ulceração da boca e do revestimento interno do intestino
- Tosse
- Dor de garganta
- Perda de cabelo
- Irritação na pele
- Fígado dilatado
- Emagrecimento dos ossos
- Dor no local da injeção
- Inflamação dos vasos sanguíneos
- Queda nas plaquetas (células envolvidas na coagulação) - com risco aumentado de sangramento ou hematomas
Eventos adversos incomuns (afetam até 1 em 100 pacientes)
- Dor não especificada
- Presença de sangue ou proteína na urina
Eventos adversos raros (afetam até 1 em 1.000 pacientes)
- Danos hepáticos causados pelo bloqueio das pequenas veias do fígado (doença veno-oclusiva)
- Uma mudança na regulação de fluidos no corpo que pode levar ao inchaço
Eventos adversos muito raros (afetam até 1 em 10.000 pacientes)
- Radiografia de raios-x anormal dos pulmões (infiltração pulmonar)
- Lesões de cor violeta, elevadas e dolorosas nos membros e às vezes no rosto e pescoço, associadas a febre (síndrome de Sweet)
- Inflamação dos vasos sanguíneos da pele (vasculite cutânea) • Agravamento da artrite reumatoide já presente
- Mudança incomum na urina
Frequência desconhecida (a frequência não pode ser estimada a partir dos dados disponíveis)
- Inchaço e dor nas articulações, como na gota (pseudogota).
A doença enxerto contra hospedeiro (GvHD) pode ocorrer em pacientes submetidos à doação de células-tronco ou transplante de medula óssea - esta é uma reação das células do doador em relação à pessoa que recebe o transplante; sinais e sintomas incluem erupção nas palmas das mãos ou plantas dos pés e úlceras e feridas na boca, intestinos, fígado, pele ou olhos, pulmões, vagina e articulações. Alguns casos de GvHD foram fatais.
Os eventos adversos que você pode experimentar se você for um doador de células-tronco para outra pessoa são:
Eventos adversos muito comuns (afetam mais de 1 em 10 pacientes)
- Dor de cabeça
- Dor nos ossos ou músculos. Pergunte ao seu médico qual medicamento tomar para aliviar este
- Alterações nos glóbulos brancos ou plaquetas (o seu médico irá avaliá-los com análises ao sangue)
Eventos adversos comuns (afetam até 1 em 10 pacientes)
- Aumento dos níveis de algumas enzimas hepáticas (seu médico irá monitorá-las)
Eventos adversos incomuns (afetam até 1 em 100 pacientes)
- Reação alérgica grave
- Problemas com o baço
- Níveis aumentados de ácido úrico que podem ocorrer com a gota
- Piora da artrite reumatóide
Relatório de efeitos colaterais
Se tiver quaisquer efeitos secundários, fale com o seu médico ou farmacêutico ou enfermeiro. Isto inclui quaisquer efeitos secundários possíveis não listados neste folheto. Também pode comunicar os efeitos secundários diretamente através do sistema nacional de notificação listado no Apêndice V.
Expiração e retenção
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após o prazo de validade impresso na embalagem exterior e no rótulo da seringa após a abreviatura EXP / EXP.O prazo de validade corresponde ao último dia do mês.
Conservar e transportar refrigerado (2 ° C - 8 ° C). Não congele. Manter a seringa pré-cheia na embalagem original para proteger o medicamento da luz.
A seringa pode ser mantida fora do refrigerador e deixada em temperatura ambiente por um único período de até 7 dias (porém, não acima de 25 ° C).
Não use Nivestim se notar que está turvo ou contém partículas.
Não deite fora quaisquer medicamentos na canalização ou no lixo doméstico. Pergunte ao seu farmacêutico como deitar fora os medicamentos que já não utiliza. Isto ajudará a proteger o ambiente.
Outra informação
O que Nivestim contém
- O ingrediente ativo é filgrastim. Cada mililitro contém 60 milhões de unidades [MU] (600 microgramas) ou 96 milhões de unidades [MU] (960 microgramas) de filgrastim.
- Nivestim 12 MU / 0,2 ml solução injetável / perfusão: cada seringa pré-cheia contém 12 milhões de unidades (MU), 120 microgramas de filgrastim em 0,2 ml (correspondendo a 0,6 mg / ml).
- Nivestim 30 MU / 0,5 ml solução injetável / para perfusão: Cada seringa pré-cheia contém 30 milhões de unidades (MU), 300 microgramas de filgrastim em 0,5 ml (correspondendo a 0,6 mg / ml).
- Nivestim 48 MU / 0,5 ml solução injetável / para perfusão: Cada seringa pré-cheia contém 48 milhões de unidades (MU), 480 microgramas de filgrastim em 0,5 ml (correspondendo a 0,96 mg / ml).
- Os outros componentes são ácido acético (glacial), hidróxido de sódio, sorbitol E420, polissorbato 80 e água para preparações injetáveis.
Qual a aparência de Nivestim e conteúdo da embalagem
O Nivestim é uma solução injetável / para perfusão límpida e incolor em seringa pré-cheia com uma agulha protetora para injeção (aço inoxidável). Cada embalagem pode conter 1, 5, 8 ou 10 seringas.
Instruções ao paciente para autoinjeção
Esta seção contém informações sobre como injetar Nivestim em si mesmo. É importante que não tente injetar o medicamento sozinho antes de receber uma formação específica do seu médico ou enfermeiro.
Também é importante que elimine a seringa num recipiente à prova de picada de agulha.Se tiver quaisquer questões ou preocupações sobre a auto-injecção, fale com o seu médico ou enfermeiro.
Como faço para me injetar?
Normalmente, o Nivestim é administrado duas vezes ao dia por injeção, nos tecidos localizados sob a pele, também conhecida como injeção subcutânea.
Aprender o procedimento de autoinjeção significa evitar ficar em casa esperando a chegada da enfermeira e muito menos ter que ir ao hospital ou clínica todos os dias para receber a injeção.
Terá de se injectar à mesma hora todos os dias. Os locais mais adequados para injetar são:
- a frente da coxa,
- o abdômen, exceto para a área ao redor do umbigo.
É melhor mudar sempre o local da injeção todos os dias para evitar dores numa determinada área.
Equipamento necessário para administração
O seguinte equipamento é necessário ao realizar uma "auto-injeção subcutânea:"
- Uma nova seringa pré-cheia de Nivestim.
- Um recipiente para objetos cortantes (à prova de perfuração da agulha) para descartar com segurança as seringas usadas.
- Toalhetes anti-sépticos (se recomendados pelo seu médico ou enfermeiro).
Como faço para administrar Nivestim por autoinjeção subcutânea?
- Tente injetar-se aproximadamente à mesma hora todos os dias.
- Retire a seringa de Nivestim do frigorífico e deixe-a atingir a temperatura ambiente (cerca de 25 ° C). Isto demorará 15-30 minutos. Verifique a data na embalagem para se certificar de que o medicamento não expirou. Tenha o recipiente para a colheita de materiais residuais pontiagudos nas proximidades.
- Procure um local de trabalho bem iluminado para a injeção e verifique a dose prescrita.
- Lave bem as mãos com água e sabão.
- Retire a seringa do blister e verifique se a solução que contém é límpida, incolor e praticamente isenta de partículas visíveis. Não use a seringa de Nivestim se o líquido contiver partículas flutuantes ou se algum líquido vazar da seringa.
- Segure a seringa com a agulha apontando para cima. Retire a tampa protetora da agulha. A seringa está pronta para ser usada. Pode haver uma pequena bolha de ar na seringa. Não é necessário remover a bolha de ar antes de injetar. Injetar a solução na presença de uma bolha de ar não é perigoso.
- Decida onde injetar o Nivestim - localize um local na parte frontal do abdómen ou uma parte da frente das coxas.Escolha um local de injeção diferente de cada vez. Não escolha uma área dolorida, vermelha, com hematomas ou cicatrizes. Se sua enfermeira ou médico recomendar, limpe a superfície da pele com um desinfetante.
- Faça uma "dobra de pele larga entre o polegar e o indicador, tomando cuidado para não tocar na área que acabou de limpar".
- Com a outra mão, insira a agulha sob a pele em um ângulo de aproximadamente 45 °.
- Puxe o êmbolo levemente para verificar se nenhum sangue entra na seringa. Se vir sangue na seringa, retire a agulha e insira-a em outro lugar.Lentamente empurre o êmbolo até que todo o conteúdo da seringa tenha sido esvaziado.
- Após injetar a solução, remova a agulha da pele.
- Seguindo as instruções abaixo para o dispositivo protetor de agulha ativo ou passivo, certifique-se de que o dispositivo cobre a agulha.
- Retorne a seringa para o recipiente para objetos cortantes. Não tente recolocar a tampa protetora.
- Mantenha as seringas usadas fora do alcance e da vista das crianças.
- NUNCA jogue seringas no seu recipiente de lixo doméstico.
Lembrar
A maioria das pessoas pode aprender sobre a autoinjeção subcutânea, mas se você tiver muitas dificuldades, não tenha medo de pedir ajuda e conselho ao seu médico ou enfermeiro.
Usando o Active Ultrasafe Needle Guard para Nivestim 12 MU / solução de 0,2 ml para injeção / infusão
A seringa pré-cheia está equipada com um dispositivo de segurança da agulha, UltraSafe Needle Guard, que protege contra a picada acidental da agulha.Ao manusear a seringa pré-cheia, mantenha as mãos atrás da agulha.
- Efectue a injecção de acordo com a técnica acima descrita.
- Quando terminar a injeção, deslize a proteção da agulha para a frente até que a agulha esteja completamente coberta (o dispositivo se encaixe no lugar).
Uso do protetor de agulha Ultrasafe Passive para Nivestim 30 MU / 0,5 ml solução injetável / infusão e Nivestim 48 MU / 0,5 ml solução injetável / infusão
A seringa pré-cheia está equipada com uma proteção de segurança da agulha, UltraSafe Needle Guard, que protege contra a picada acidental da agulha.Ao manusear a seringa pré-cheia, mantenha as mãos atrás da agulha.
- Efectue a injecção de acordo com a técnica acima descrita.
- Enquanto segura a seringa com os dedos apoiados na extremidade de suporte, aplique pressão no êmbolo até que a injeção de toda a dose esteja concluída. O sistema passivo de proteção da agulha NÃO será ativado se a dose COMPLETA não tiver sido administrada.
- Remova a agulha da pele e, em seguida, solte o êmbolo e a seringa avançará até que a proteção cubra a agulha e se encaixe no lugar.
AS SEGUINTES INFORMAÇÕES DESTINAM-SE APENAS A MÉDICOS OU PROFISSIONAIS DE SAÚDE
Nivestim não contém conservantes. Devido ao risco de contaminação bacteriana, as seringas Nivestim destinam-se a uma única utilização.
A exposição acidental a temperaturas de congelamento até 24 horas não tem efeitos adversos na estabilidade de Nivestim.A seringa pré-cheia congelada pode ser descongelada e devolvida ao frigorífico para utilização posterior. Se a exposição a baixas temperaturas for superior a 24 horas ou se congelado por mais de uma vez, o Nivestim NÃO deve ser usado mais.
Nivestim não deve ser diluído em solução de cloreto de sódio. Este medicamento não deve ser misturado com outros medicamentos, exceto os descritos abaixo. Se não for diluído conforme descrito abaixo, o filgrastim diluído pode ser absorvido em vidro e materiais plásticos.
Se necessário, Nivestim pode ser diluído em solução de glicose a 50 mg / ml (5%) para perfusão. A diluição para concentrações finais <0,2 MU (2 microgramas) por ml nunca é recomendada. A solução deve ser inspecionada visualmente antes do uso. Apenas soluções límpidas sem partículas visíveis devem ser usadas. Para pacientes tratados com filgrastim diluído para concentrações abaixo de 1,5 MU (15 microgramas) por mL, albumina sérica humana (HSA) para uma concentração final de 2 mg / ml.
Exemplo: Em um volume final a ser injetado de 20 mL, doses totais de filgrastim abaixo de 30 MU (300 microgramas) devem ser administradas adicionando 0,2 mL de uma solução de albumina humana 200 mg / mL (20%). Diluído com solução de glicose 50 mg / ml (5%) para perfusão, Nivestim é compatível com vidro e vários materiais plásticos como PVC, poliolefina (um copolímero de polipropileno e polietileno) e polipropileno.
Após diluição: A estabilidade química e física em uso da solução diluída para perfusão foi demonstrada durante 24 horas a 2 ° C a 8 ° C. Do ponto de vista microbiológico, o produto deve ser usado imediatamente. Se não for usado imediatamente, os tempos de armazenamento em uso e as condições anteriores ao uso são de responsabilidade do usuário e normalmente não excedem 24 horas a 2 ° C a 8 ° C, a menos que a diluição tenha ocorrido em condições assépticas controladas e validadas.
Folheto Informativo Fonte: AIFA (Agência Italiana de Medicamentos). Conteúdo publicado em janeiro de 2016. As informações apresentadas podem não estar atualizadas.
Para ter acesso à versão mais atualizada, é aconselhável acessar o site da AIFA (Agência Italiana de Medicamentos). Isenção de responsabilidade e informações úteis.
01.0 NOME DO MEDICAMENTO
SOLUÇÃO NIVESTIM 12 MU / 0,2 ML PARA INJEÇÃO / INFUSÃO
02.0 COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Cada ml de solução injetável ou perfusão contém 60 milhões de unidades [MU] (600 mcg) de filgrastim *.
Cada seringa pré-cheia contém 12 milhões de unidades (MU) (120 mcg) de filgrastim em 0,2 mL (0,6 mg / mL).
* fator estimulador de colônia de granulócitos de metionina recombinante [GCSF]) produzido em Escherichia Coli (BL21) com tecnologia de DNA recombinante.
Excipiente (s) com efeito conhecido
Cada ml de solução contém 50 mg de sorbitol.
Para a lista completa de excipientes, consulte a seção 6.1.
03.0 FORMA FARMACÊUTICA
Solução para injeção / infusão.
Solução límpida e incolor.
04.0 INFORMAÇÕES CLÍNICAS
04.1 Indicações terapêuticas
Filgrastim é indicado para a redução da duração da neutropenia e a incidência de neutropenia febril em pacientes tratados com quimioterapia citotóxica padrão para doenças malignas (com exceção de leucemia mieloide crônica e síndromes mielodisplásicas) e redução da duração da neutropenia em pacientes submetidos a terapia mieloablativa seguida de transplante de medula óssea considerada de alto risco para neutropenia grave prolongada.
A segurança e eficácia do filgrastim são semelhantes em adultos e crianças submetidos à quimioterapia citotóxica.
Filgrastim é indicado para a mobilização de células progenitoras do sangue periférico (PBPCs).
Em pacientes, crianças ou adultos com neutropenia congênita, cíclica ou idiopática grave, com uma contagem absoluta de neutrófilos (ANC) ≤ 0,5 x 109 / L e uma história de infecções graves ou recorrentes, a administração a longo prazo de filgrastim é indicada para aumentar os neutrófilos contagens e reduzindo a incidência e duração dos eventos relacionados à infecção.
Filgrastim é indicado para o tratamento da neutropenia persistente (ANC menor ou igual a 1,0 x 109 / l) em pacientes com infecção avançada por HIV para reduzir o risco de infecções bacterianas quando outras opções de tratamento são inadequadas.
04.2 Posologia e método de administração
A terapia com filgrastim só deve ser realizada em conjunto com um centro de câncer com
ter experiência em tratamento e hematologia com G-CSF e ter o equipamento de diagnóstico necessário. Os procedimentos de mobilização e aférese devem ser realizados em colaboração com um centro de oncologia-hematologia com experiência aceitável na área e onde o monitoramento de células progenitoras hematopoiéticas possa ser realizado corretamente.
Dosagem
Quimioterapia citotóxica padrão
A dose recomendada de filgrastim é de 0,5 MU (5 mcg) / kg / dia. A primeira dose de filgrastim deve ser administrada pelo menos 24 horas após a quimioterapia citotóxica.
A dosagem diária de filgrastim deve continuar até que o nadir de neutrófilos esperado tenha sido excedido e a contagem de nuetrófilos tenha retornado a um nível normal. Após a quimioterapia padrão para tumores sólidos, linfomas e leucemias linfoides, a duração necessária do tratamento para atender a esses critérios pode chegar a 14 dias Após o tratamento de indução e consolidação na leucemia mieloide aguda, a duração do tratamento pode ser consideravelmente mais longa (até 38 dias), dependendo do tipo, dose e padrão de quimioterapia citotóxica utilizada.
Em pacientes submetidos à quimioterapia citotóxica, um aumento transitório na contagem de neutrófilos é tipicamente observado 1-2 dias após o início da terapia com filgrastim. O nadir esperado de neutrófilos não foi excedido e a contagem de neutrófilos não voltou ao nível normal. A descontinuação prematura da terapia com filgrastim antes de o nadir de neutrófilos esperado ser atingido não é recomendada.
Pacientes em terapia mieloablativa seguida de transplante de medula óssea
A dose inicial recomendada de filgrastim é 1,0 MU (10 mcg) / kg / dia.
A primeira dose de Filgrastim deve ser administrada pelo menos 24 horas após a quimioterapia citotóxica e pelo menos 24 horas após a perfusão da medula óssea.
Assim que o nadir dos neutrófilos for ultrapassado, a dose diária de Filgrastim deve ser titulada com base na resposta dos neutrófilos da seguinte forma:
Mobilização de PBPCs
Para a mobilização de células progenitoras de sangue periférico (PBPCs) em pacientes submetidos a terapia mielossupressora ou mieloablativa seguida de transplante autólogo de células progenitoras de sangue periférico
A dose recomendada de filgrastim para mobilização de PBPC, quando usado sozinho, é de 1,0 MU (10 mcg) / kg / dia por 5 a 7 dias consecutivos. Planejamento de leucaferese: geralmente é suficiente 1 ou 2 leucaferese nos dias 5 e 6. Em outros casos, pode ser necessária leucaferese adicional. A administração de filgrastim deve ser continuada até a última leucaferese.
A dose recomendada de filgrastim para mobilização de PBPC após a quimioterapia mielossupressora é de 0,5 MU (5 mcg) / kg / dia a ser administrada diariamente a partir do primeiro dia após a conclusão da quimioterapia até que o nadir de neutrófilos esperado tenha sido excedido e a contagem de neutrófilos não tenha retornado a um nível normal. A leucaferese deve ser realizada durante o período em que a ANC aumenta de 5,0 x 109 / L. Em pacientes que não estão sendo submetidos a quimioterapia extensa, uma única leucaferese costuma ser suficiente. Em outros casos, é recomendada mais leucaferese.
Para a mobilização de células progenitoras de sangue periférico (PBPCs) em doadores saudáveis antes do transplante de células progenitoras de sangue periférico alogênico
Para a mobilização de PBPC em dadores saudáveis, o filgrastim deve ser administrado por injeção subcutânea na dose de 10 mcg / kg / dia durante 4 a 5 dias consecutivos. A leucaferese deve começar no dia 5 e continuar conforme necessário até o dia 6 para atingir 4 x 106 células CD34 + / kg de peso corporal do receptor.
Em pacientes com neutropenia crônica grave
Neutropenia congênita: a dose recomendada é de 1,2 MU (12 microgramas) / kg / dia em dose única ou em doses divididas.
Neutropenia idiopática ou cíclica: a dose inicial recomendada é de 0,5 MU (5 mcg) / kg / dia em dose única ou em doses divididas.
Ajustes de dosagem: Filgrastim deve ser administrado diariamente até que a contagem de neutrófilos seja atingida e possa ser mantida acima de 1,5 x 109 / l. Quando a resposta é obtida, a menor dose efetiva para manter esse nível deve ser determinada. A administração diária a longo prazo é necessária para manter contagens adequadas de neutrófilos. Após uma a duas semanas de terapia, a dose inicial pode ser dobrada ou reduzida pela metade com base na resposta do paciente. Depois disso, a dose pode ser ajustada individualmente a cada 1-2 semanas para manter uma contagem média de neutrófilos entre 1,5 x 109 / L e 10 x 109 / L. Em pacientes com infecções graves, um esquema mais rápido de aumento progressivo da dose pode ser considerado. Em estudos clínicos, 97% dos respondedores alcançaram uma resposta completa com doses ≤ 24 mcg / kg / dia. Não foi demonstrada a segurança a longo prazo da administração de filgrastim em doses superiores a 24 microgramas / kg / dia em doentes com neutropenia crónica grave.
Em pacientes com infecção por HIV
Reversão da neutropenia
A dose inicial recomendada de filgrastim é de 0,1 MU (1 micrograma) / kg / dia administrada diariamente com titulação até um máximo de 0,4 MU (4 mcg) / kg / dia até que seja alcançada e possa uma contagem normal de nuetrófilos (ANC> 2,0 x109 / l) ser mantido. Em estudos clínicos,> 90% dos pacientes responderam a essas doses, conseguindo reversão da neutropenia em uma mediana de 2 dias.
Em um pequeno número de pacientes (
Manter uma contagem normal de neutrófilos
Quando a reversão da neutropenia for alcançada, a menor dose eficaz para manter uma contagem normal de neutrófilos deve ser determinada. Recomenda-se um ajuste de dose inicial com dosagem em dias alternados de 30 MU (300 mcg) / dia. Podem ser necessários ajustes de dose adicionais, dependendo do ANC do paciente, a fim de manter a contagem de neutrófilos em> 2,0 x 109 / L. Em ensaios clínicos, foram necessárias doses de 30 MU (300 mcg) / dia. 1 a 7 dias por semana. manter ANC> 2,0 x 109 / L, com uma frequência mediana de administração de 3 dias por semana. A administração a longo prazo pode ser necessária para manter ANC> 2,0 x 109 / L.
Populações especiais
Pacientes idosos
Apenas um pequeno número de pacientes idosos foi incluído em ensaios clínicos com filgrastim. Nenhum estudo específico foi realizado nesta população de pacientes. Portanto, nenhuma recomendação de dosagem específica pode ser feita para esses pacientes.
Pacientes com insuficiência renal ou hepática
Os estudos realizados com filgrastim em doentes com compromisso renal ou hepático grave mostram que o seu perfil farmacocinético e farmacodinâmico é semelhante ao observado em indivíduos saudáveis. Nestes casos, nenhum ajuste de dosagem é necessário.
Pacientes pediátricos com neutropenia crônica grave (SCN) e doenças malignas
Em ensaios clínicos, sessenta e cinco por cento dos pacientes tratados para um SCN tinham menos de 18 anos. Neste grupo etário, incluindo principalmente doentes com neutropenia congénita, a eficácia foi demonstrada.Não foram observadas diferenças nos perfis de segurança dos doentes pediátricos tratados para neutropenia crónica grave.
Os dados de ensaios clínicos com pacientes pediátricos indicam que a segurança e eficácia do filgrastim são semelhantes em adultos e crianças submetidos à quimioterapia citotóxica.
As recomendações de dosagem em pacientes pediátricos são idênticas às recomendações válidas para adultos submetidos à quimioterapia citotóxica mielossupressora.
Método de administração
Quimioterapia citotóxica padrão
Filgrastim pode ser administrado por injeção subcutânea diária ou perfusão intravenosa diária diluída em solução injetável de glicose 50 mg / ml (5%) durante 30 minutos (ver secção 6.6 sobre instruções de diluição). Na maioria dos casos, a via subcutânea é preferível. Há evidências de um estudo de dose única de que o uso intravenoso pode reduzir a duração do efeito. A relevância clínica deste achado para a administração de doses múltiplas não é clara. A escolha da via de administração deve ser baseada na condição clínica de cada paciente. Em ensaios clínicos randomizados, foram utilizadas doses subcutâneas de 230 mcg / m2 / dia (4,0 a 8,4 mcg / kg / dia).
Pacientes em terapia mieloablativa seguida de transplante de medula óssea
Filgrastim é administrado por perfusão intravenosa com a duração de 30 minutos ou por perfusão intravenosa ou por perfusão subcutânea contínua de 24 horas. Filgrastim deve ser diluído em 20 ml de uma solução de glicose a 50 mg / ml (5%) para perfusão (ver secção 6.6).
Mobilização de PBPCs
Para a mobilização de células progenitoras de sangue periférico (PBPC) em pacientes submetidos a terapia mielossupressora ou mieloablativa seguida por transplante autólogo de células progenitoras de sangue periférico, a dose recomendada de filgrastim por infusão subcutânea contínua pode ser administrada durante 24 horas ou por injeção subcutânea única diária por 5 - 7 dias consecutivos. Para a perfusão, o filgrastim deve ser diluído em 20 ml de uma solução injectável de glucose 50 mg / ml (5%) (ver secção 6.6).
Infecção por NCG / HIV
Injeção subcutânea.
Para obter instruções sobre o manuseio do medicamento antes do uso, consulte a seção 6.6.
04.3 Contra-indicações
Hipersensibilidade à substância ativa ou a qualquer um dos excipientes mencionados na secção 6.1.
04.4 Advertências especiais e precauções adequadas de uso
Avisos especiais
Filgrastim não deve ser usado para aumentar a dose de quimioterapia citotóxica além do regime de dose padrão.
O filgrastim não deve ser utilizado em doentes com neutropenia congénita grave (síndrome de Kostman) com anomalias citogenéticas.
Reações de hipersensibilidade, incluindo reações anafiláticas, que ocorrem no início ou após o tratamento, foram relatadas em pacientes tratados com filgrastim. Descontinuar permanentemente o tratamento com filgrastim em pacientes com hipersensibilidade clinicamente significativa.Não administre filgrastim a pacientes com história de hipersensibilidade ao filgrastim ou pegfilgrastim.
Tal como acontece com todas as proteínas terapêuticas, existe um risco potencial de imunogenicidade. A probabilidade de gerar anticorpos contra filgrastim é geralmente baixa. O desenvolvimento de anticorpos de ligação é esperado com todos os produtos biológicos; no entanto, até o momento, eles não foram associados à atividade. Neutralizante.
Proliferação de células malignas
O GCSF pode promover a proliferação de células mieloides em vitro e efeitos semelhantes podem ser vistos em vitro em algumas células não mieloides.
A segurança e eficácia da administração de Filgrastim a pacientes com síndrome mielodisplásica ou leucemia mielóide crônica não foram demonstradas.
Filgrastim não é indicado nessas situações. Deve-se prestar atenção especial ao diagnóstico diferencial entre a transformação de blastos na leucemia mieloide crônica e na leucemia mieloide aguda.
Devido aos dados limitados sobre segurança e eficácia, o filgrastim deve ser administrado com cautela em pacientes com LMA secundária.
A segurança e eficácia da administração de filgrastim em pacientes com idade de novo e citogenética favorável [t (8; 21), t (15; 17) e inv] não foram demonstradas.
Outras precauções especiais
O monitoramento da densidade óssea pode ser indicado em pacientes com osteoporose subjacente que estão em terapia contínua com filgrastim por mais de 6 meses.
Foram relatadas reações adversas pulmonares raras (> 0,01% e pneumonia intersticial após a administração de G-CSF. Pacientes com história recente de infiltração pulmonar ou pneumonia podem estar em risco aumentado. O aparecimento de sinais pulmonares, como tosse, febre e dispneia em a associação com sinais radiológicos de infiltração pulmonar e deterioração da função pulmonar podem ser sinais preliminares de síndrome da dificuldade respiratória do adulto (SDRA) .Filgrastim deve ser descontinuado e iniciado o tratamento apropriado.
A síndrome de vazamento capilar foi relatada após a administração de fator estimulador de colônias de granulócitos e é caracterizada por hipotensão, hipoalbuminemia, edema e hemoconcentração. Os doentes que desenvolvem sintomas de síndrome de fuga capilar devem ser cuidadosamente monitorizados e receber tratamento sintomático padrão, que pode incluir a necessidade de cuidados intensivos (ver secção 4.8).
Precauções especiais em pacientes com câncer
Leucocitose
Contagens de leucócitos de 100 x 109 / L ou mais foram observadas em menos de 5% dos pacientes tratados com filgrastim em doses acima de 0,3 MU / kg / dia (3 mcg / kg / dia). Não foram observadas reações adversas diretamente atribuíveis a este grau de leucocitose. No entanto, tendo em conta os riscos potenciais associados à leucocitose grave, deve ser efectuada uma monitorização regular da contagem dos glóbulos brancos durante a terapêutica com filgrastim. O tratamento com filgrastim deve ser interrompido imediatamente se a contagem de glóbulos brancos exceder 50 x 109 / l após o nadir esperado. No entanto, durante o período de administração de filgrastim para mobilização de PBPC, o tratamento deve ser interrompido ou a dose reduzida se a contagem de leucócitos exceder 70 x 109 / l.
Riscos associados à quimioterapia em altas doses
Deve-se ter cuidado especial no tratamento de pacientes com quimioterapia em altas doses, porque uma resposta tumoral mais favorável não foi demonstrada e porque a administração de quimioterapia em altas doses pode aumentar os efeitos tóxicos, incluindo efeitos cardíacos, pulmonares, neurológicos e dermatológicos. (consulte o resumo das características do produto dos agentes quimioterápicos utilizados).
O tratamento com filgrastim isoladamente não previne a trombocitopenia e a anemia após quimioterapia mielossupressora. Como resultado da possibilidade de receber doses mais elevadas de quimioterapia (por exemplo, doses completas de acordo com o regime de dosagem prescrito), o paciente pode ser exposto a um risco aumentado de trombocitopenia e anemia. Recomenda-se, portanto, a verificação regular da contagem de plaquetas e do hematócrito, devendo ser dada atenção especial durante a administração, tanto isoladamente quanto em combinação, de agentes quimioterápicos conhecidos por induzirem trombocitopenia grave.
O uso de PBPCs mobilizados com filgrastim demonstrou reduzir a gravidade e a duração da trombocitopenia após quimioterapia mielossupressora ou mieloablativa.
Esplenomegalia
Foram notificados casos pouco frequentes de esplenomegalia e ruptura esplénica após a administração de filgrastim. Alguns casos de ruptura esplênica foram fatais. Os indivíduos que receberam filgrastim e relataram dor abdominal superior esquerda e / ou dor na extremidade do ombro devem ser avaliados para aumento do baço ou ruptura esplênica.
Outras precauções especiais
O efeito do filgrastim em pacientes com progenitores mieloides significativamente reduzidos não foi estudado. Para aumentar a contagem de neutrófilos, o filgrastim atua principalmente nos precursores de neutrófilos. Portanto, em pacientes com baixo número de precursores (por exemplo, em pacientes tratados com radioterapia ou quimioterapia extensa ou pacientes com infiltração tumoral da medula óssea), a resposta dos neutrófilos pode ser reduzida.
Foram notificados casos de doença enxerto contra hospedeiro, GvHD e morte em doentes tratados com G-CSF após transplante alogénico de medula óssea (ver secção 5.1).
O efeito do filgrastim na doença de GvHD não foi definido.
O aumento da atividade hematopoiética da medula óssea em resposta à terapia com fator de crescimento foi associado a achados de imagem óssea positivos transitórios. Isso deve ser considerado ao interpretar os relatórios ósseos.
Precauções especiais em pacientes submetidos à mobilização de células progenitoras do sangue periférico.
Mobilização
Não há estudos radiológicos prospectivos comparando os dois métodos de mobilização recomendados (filgrastim sozinho ou em combinação com quimioterapia mielossupressora) na mesma população de pacientes. O grau de variabilidade entre pacientes individuais e entre os testes laboratoriais de células CD34 + demonstra a dificuldade de comparar diferentes estudos, portanto, é difícil recomendar um método ideal. A escolha do método de mobilização deve ser avaliada em relação aos objetivos individuais do tratamento do paciente.
Exposição anterior a agentes citotóxicos
Em pacientes extensivamente pré-tratados com terapia mielossupressora, é possível que a mobilização de PBPC não seja suficiente para obter o número mínimo recomendado de células (2,0 x 106 células CD34 + / kg) ou que a aceleração da recuperação plaquetária seja menos acentuada.
Alguns agentes citotóxicos apresentam toxicidade particular nas células progenitoras hematopoiéticas e podem neutralizar sua mobilização. Substâncias como melfalano, carmustina (BCNU) e carboplatina, se administradas por um período prolongado antes da mobilização das células progenitoras, podem reduzir o número de células coletadas. No entanto, a administração de melfalano, carboplatina ou BCNU em combinação com filgrastim demonstrou ser eficaz na mobilização de células progenitoras. Se um transplante de células progenitoras de sangue periférico for planejado, a mobilização de células-tronco deve ser planejada na fase inicial do tratamento pretendido do paciente. Deve-se prestar atenção especial ao número de células progenitoras mobilizadas em tais pacientes antes da administração de quimioterapia em altas doses. Se a coleta de células for inadequada de acordo com os critérios de avaliação previamente indicados, tratamentos alternativos que não requeiram o uso de células progenitoras devem ser considerados.
Avaliação da coleta de células progenitoras
Na avaliação quantitativa de células progenitoras obtidas em pacientes tratados com filgrastim, deve ser dada atenção especial ao método de contagem. Os resultados da contagem de células CD34 + por citometria de fluxo variam de acordo com a metodologia utilizada; portanto, os números derivados de estudos conduzidos em outros laboratórios devem ser interpretados com cautela.
A análise estatística da relação entre o número de células CD34 + reinfundidas e a taxa de recuperação plaquetária após a quimioterapia de alta dose indica uma relação complexa, mas constante.
A recomendação de coletar um número mínimo de 2,0 x 106 células CD34 + / kg é baseada na experiência publicada, o que indica que a recuperação hematológica é, portanto, adequada. Quantidades maiores do que o número mínimo indicado parecem estar relacionadas a uma recuperação mais rápida, e quantidades menores a uma recuperação mais lenta.
Precauções especiais em doadores saudáveis submetidos à mobilização de células progenitoras do sangue periférico
A mobilização de PBPC não tem benefício clínico direto em doadores saudáveis e só deve ser considerada com o objetivo de transplante alogênico de células-tronco.
A mobilização de PBPC só deve ser considerada em doadores que atendam aos critérios de elegibilidade clínicos e laboratoriais normais para doação de células-tronco, com atenção especial aos parâmetros hematológicos e à presença de doenças infecciosas.
A segurança e eficácia do filgrastim não foram avaliadas em dadores saudáveis com 60 anos de idade.
Trombocitopenia transitória (plaquetas
Se mais de uma leucaferese for necessária, doadores com plaquetas
A leucaferese não deve ser realizada em dadores sob terapia anticoagulante ou que apresentem alterações conhecidas na hemostasia.
A administração de filgrastim deve ser descontinuada ou a posologia deve ser reduzida se a contagem de glóbulos brancos atingir> 70 x109 / l.
Os doadores que recebem G-CSF para mobilização de PBPC devem ser monitorados até que os parâmetros hematológicos sejam normalizados.
Após o uso de G-CSF em dadores saudáveis, foram observadas alterações citogênicas transitórias, mas o significado dessas alterações é desconhecido.
O acompanhamento de segurança de longo prazo em doadores está em andamento. No entanto, o risco de desenvolver um clone de células mieloides malignas não pode ser excluído. Recomenda-se que o centro de aférese realize o registro e triagem sistemáticos de doadores de células-tronco para garantir o monitoramento de segurança a longo prazo.
Após a administração de G-CSF, geralmente foi observada esplenomegalia assintomática e, em casos muito raros, ruptura do baço em doadores (e pacientes) saudáveis. Alguns casos de ruptura do baço foram fatais. Portanto, o volume do baço deve ser verificado cuidadosamente (por exemplo, por exame físico, ultrassom). O diagnóstico de ruptura do baço deve ser considerado em doadores e / ou pacientes com dor abdominal superior esquerda ou dor na omoplata.
Na experiência pós-comercialização, eventos adversos pulmonares (hemoptise, hemorragia pulmonar, infiltração pulmonar, dispneia e hipóxia) foram relatados muito raramente em dadores normais após o uso de outros medicamentos contendo filgrastim. Em caso de suspeita de eventos adversos pulmonares ou estabelecido, descontinuação de tratamento com filgrastim deve ser considerado e a assistência médica necessária fornecida.
Precauções especiais em recipientes de células progenitoras de sangue periférico alogênico mobilizadas com filgrastim
Os dados atuais indicam que as interações imunológicas entre as PBPCs alogênicas e o receptor podem estar associadas a um risco aumentado de doença do enxerto versus hospedeiro aguda e crônica (GvHD) em comparação com o transplante de medula óssea.
Precauções especiais em pacientes com neutropenia crônica grave (SCN)
Hemograma completo
A contagem de plaquetas deve ser monitorada com frequência, particularmente durante as primeiras semanas de terapia com filgrastim. A descontinuação intermitente do tratamento ou redução da dose de filgrastim deve ser considerada em pacientes que desenvolvem trombocitopenia, ou seja, com plaquetas
Outras alterações no hemograma podem ocorrer, incluindo anemia e aumentos transitórios nos progenitores mieloides, que requerem monitoramento cuidadoso dos hemogramas.
Transformação em leucemia ou síndrome mielodisplásica
Deve-se prestar atenção especial ao diagnóstico diferencial entre neutropenia crônica grave e outras doenças hematológicas, como anemia aplástica, mielodispalsia e leucemia mielóide. Um hemograma completo com contagem diferencial e de plaquetas, bem como uma avaliação da morfologia da medula óssea e um cariótipo devem ser feitos antes de iniciar o tratamento.
Síndromes mielodisplásicas (SMD) ou leucemia foram observadas em um pequeno número (aproximadamente 3%) dos pacientes com neutropenia crônica grave tratados com filgrastim em ensaios clínicos. Isso só foi observado em pacientes com neutropenia congênita. MDS e leucemia são complicações naturais da doença e não devem ser considerados com certeza em relação ao tratamento com filgrastim. Anormalidades, incluindo monossomia 7, foram subsequentemente encontradas em aproximadamente 12% dos pacientes com citogenética normal na linha de base durante a repetição do teste de rotina. Se os pacientes com neutropenia crônica grave desenvolverem anormalidades citogenéticas, os riscos e benefícios de continuar o tratamento com filgrastim devem ser cuidadosamente considerados; A administração de filgrastim deve ser interrompida se houver desenvolvimento de SMD ou leucemia. Atualmente, não se sabe se o tratamento de longo prazo de pacientes com neutropenia crônica grave pode predispor os pacientes a anormalidades citogenéticas, SMD ou transformação leucêmica. Nestes pacientes, análises morfológicas e citogenéticas da medula óssea são recomendadas em intervalos regulares (aproximadamente a cada 12 meses).
Esplenomegalia
Foram notificados casos pouco frequentes de esplenomegalia e ruptura esplénica após a administração de filgrastim. Alguns casos de ruptura esplênica foram fatais. Os indivíduos que receberam filgrastim e relataram dor abdominal superior esquerda e / ou dor na extremidade do ombro devem ser avaliados para aumento do baço ou ruptura esplênica.
Outras precauções especiais
As causas de neutropenia transitória, como infecções virais, devem ser excluídas.
A esplenomegalia é um efeito direto do tratamento com filgrastim. Esplenomegalia palpável foi observada em 31% dos pacientes em estudos clínicos. Aumentos de volume, medidos radiologicamente, foram observados no início da terapia com filgrastim e mostraram tendência de estabilização. As reduções de dose foram observadas para retardar ou interromper a progressão da esplenomegalia, e uma esplenectomia foi necessária em 3% dos pacientes. O volume do baço deve ser verificado regularmente. A palpação abdominal é suficiente para detectar aumentos de volume anormais.
A hematúria / proteinúria ocorreu em um pequeno número de pacientes. A urinálise deve ser realizada em intervalos regulares para detectar tais eventos.
A segurança e eficácia em recém-nascidos e em pacientes com neutropenia autoimune não foram demonstradas.
Precauções especiais em pacientes infectados com HIV
Hemograma completo
A contagem absoluta de neutrófilos (ANC) deve ser monitorada com frequência, particularmente durante as primeiras semanas de terapia com filgrastim. Alguns pacientes podem responder muito rapidamente e com um aumento acentuado na contagem de neutrófilos na dose inicial de filgrastim. Recomenda-se que o ANC seja determinado diariamente durante os primeiros 2-3 dias de administração de filgrastim.A partir daí, recomenda-se que o ANC seja determinado pelo menos duas vezes por semana durante as primeiras 2 semanas e uma vez por semana ou a cada duas semanas a partir de então. durante a terapia de manutenção. Com a administração intermitente de 30 MU (300 mcg) / dia de filgrastim, podem ocorrer grandes flutuações do ANC ao longo do tempo. Para determinar o valor mínimo ou nadir do ANC de um paciente, recomenda-se a coleta de amostras de sangue. Destinado à determinação de ANC imediatamente antes da administração pretendida de filgrastim.
Riscos associados a altas doses de medicamentos mielossupressores
O tratamento com filgrastim isoladamente não previne a trombocitopenia e a anemia após terapia mielossupressora. Uma vez que podem ser administradas doses mais elevadas ou mais destes medicamentos com o uso de filgrastim, o doente pode apresentar um risco aumentado de trombocitopenia ou anemia. Recomenda-se a monitorização regular do hematócrito (ver acima).
Infecções e doenças malignas que causam mielossupressão
A neutropenia pode ser devido à infiltração da medula óssea por infecções oportunistas, como Mycobacterium avium complexo, ou a neoplasias malignas, como linfomas. Em pacientes com infecções ou neoplasias malignas infiltrantes da medula óssea, deve-se considerar o tratamento adequado da doença subjacente, além da administração de filgrastim para o tratamento da neutropenia. Os efeitos do filgrastim na neutropenia devido a infecções ou doenças malignas que infiltram a medula óssea não foram demonstrados de forma conclusiva.
Esplenomegalia
Foram notificados casos pouco frequentes de esplenomegalia e ruptura esplénica após a administração de filgrastim. Alguns casos de ruptura esplênica foram fatais. Os indivíduos que receberam filgrastim e relataram dor abdominal superior esquerda e / ou dor na extremidade do ombro devem ser avaliados para aumento do baço ou ruptura esplênica.
Precauções especiais na anemia falciforme ou falciforme
Crises falciformes, em alguns casos fatais, foram relatadas em pacientes com doença falciforme ou falciforme tratados com filgrastim. Em pacientes com traço falciforme ou anemia falciforme, os médicos devem ter cautela ao avaliar o uso de filgrastim, que só deve ser usado após consideração cuidadosa dos benefícios e riscos potenciais.
Excipientes
Nivestim contém sorbitol. Pacientes com intolerância hereditária rara à frutose não devem usar este medicamento. Também contém menos de 1 mmol de sódio (23 mg) por dose, ou seja, é praticamente “isento de sódio”.
04.5 Interações com outros medicamentos e outras formas de interação
A segurança e eficácia do filgrastim administrado no mesmo dia da quimioterapia citotóxica mielossupressora não foram demonstradas de forma conclusiva. Como as células mielóides em divisão rápida são sensíveis à quimioterapia citotóxica mielossupressora, o uso de filgrastim não é recomendado no período. Entre 24 horas antes e 24 horas após a quimioterapia. Os dados preliminares obtidos em um pequeno número de pacientes tratados juntamente com filgrastim e 5-fluorouracil indicam que a neutropenia pode piorar.
As possíveis interações com outros fatores de crescimento hematopoiéticos e citocinas ainda não foram estudadas em ensaios clínicos.
Uma vez que o lítio promove a liberação de neutrófilos, é provável que potencialize o efeito do filgrastim. Embora essa interação não tenha sido formalmente estudada, não há evidências de que seja prejudicial.
04.6 Gravidez e lactação
Gravidez
Não existem dados ou existem dados limitados sobre a utilização de filgrastim em mulheres grávidas.
Os estudos em animais demonstraram toxicidade reprodutiva. Um "aumento da incidência de abortos espontâneos após a exposição" a múltiplos elevados de doses clínicas foi observado em coelhos
e na presença de toxicidade materna (ver secção 5.3). Foram descritos casos na literatura em que foi demonstrada a propagação placentária do filgrastim em mulheres grávidas. Filgrastim não é recomendado durante a gravidez.
Hora da alimentação
Não se sabe se o filgrastim é excretado no leite materno; portanto, filgrastim não é recomendado em mulheres que estão amamentando. Deve-se tomar uma decisão quanto a descontinuar a amamentação ou descontinuar / abster-se da terapia com filgrastim, levando em consideração o benefício da amamentação para a criança e o benefício da terapia para a mulher.
Fertilidade
Filgrastim não teve efeito sobre a reprodução ou fertilidade em ratos machos ou fêmeas (ver secção 5.3).
04.7 Efeitos sobre a capacidade de dirigir e usar máquinas
Filgrastim tem efeitos modestos na capacidade de conduzir e utilizar máquinas.Se o doente se sentir cansado, deve ter-se cuidado ao conduzir ou utilizar máquinas.
04.8 Efeitos indesejáveis
Resumo do perfil de segurança
Em ensaios clínicos, 183 doentes com cancro e 96 voluntários saudáveis foram expostos ao Nivestim.
O perfil de segurança do filgrastim observado nestes estudos clínicos foi consistente com o relatado para o medicamento de referência utilizado nestes estudos.
Em estudos clínicos em pacientes com câncer, a reação adversa atribuível ao filgrastim na dose recomendada mais frequente foi dor musculoesquelética, leve ou moderada em 10% e grave em 3% dos pacientes.
A doença de reação enxerto versus hospedeiro (GvHD) também foi relatada (ver abaixo).
Na mobilização de células-tronco circulantes periféricas (PBPCs) em dadores saudáveis, a reação adversa mais comumente relatada foi dor musculoesquelética. Leucocitose foi observada em doadores e trombocitopenia após filgrastim e leucaferese também foi observada em doadores. Esplenomegalia e ruptura esplênica também foram relatadas. Alguns casos de ruptura esplênica foram fatais.
Em doentes com neutropenia crónica grave (SCN), as reações adversas mais frequentes atribuíveis ao filgrastim foram dor óssea, dor músculo-esquelética geral e esplenomegalia.
A síndrome de vazamento capilar, que pode ser fatal se o tratamento for atrasado, foi relatada raramente (≥1 / 1000 a
Em ensaios clínicos em doentes com VIH, as únicas reações adversas consideradas exclusivamente relacionadas com a administração de filgrastim foram dor músculo-esquelética, dor óssea ligeira a moderada e mialgia. A incidência dessas reações foi semelhante à relatada em pacientes com câncer.
Tabela de reações adversas
As reações adversas listadas abaixo e a sua frequência foram observadas após o tratamento com filgrastim de acordo com dados publicados.
As frequências das reações adversas são definidas de acordo com as seguintes convenções:
Muito comum: ≥1 / 10
Comum: ≥1 / 100 y
Incomum: ≥1 / 1.000 anos
Raros: ≥1 / 10.000 anos
Muito raro:
Desconhecido: não pode ser calculado a partir dos dados disponíveis
Dentro de cada grupo de frequência, as reações adversas são apresentadas em ordem decrescente de gravidade.
Em pacientes com câncer
Doadores saudáveis submetidos à mobilização de células progenitoras de sangue periférico
Em pacientes com neutropenia crônica grave (SCN)
Em pacientes com HIV
Descrição das reações adversas selecionadas
Foram notificados GvHD e mortes em doentes a receber G-CSF após transplante alogénico de medula óssea (ver secção 5.1).
Foram notificados casos de síndrome de fuga capilar após a comercialização com a utilização de fatores estimuladores de colónias de granulócitos.Estes ocorreram geralmente em doentes com doença maligna avançada, sépsis, que estavam a tomar múltiplos fármacos de quimioterapia ou em aférese (ver secção 4.4).
Em pacientes com câncer
A dor musculoesquelética geralmente é controlada com analgésicos padrão. As reações adversas menos frequentes incluem anormalidades urinárias com disúria predominantemente leve ou moderada.
Em estudos randomizados controlados por placebo, filgrastim não aumentou a incidência de eventos adversos associados à quimioterapia citotóxica. As reações adversas observadas com igual frequência em pacientes tratados com quimioterapia com filgrastim e placebo / quimioterapia foram náuseas, vômitos, alopecia, diarreia, fadiga, anorexia , dor de cabeça, erupção na pele com tosse, dor no peito, fraqueza geral, dor de garganta, prisão de ventre e dor não especificada.
Aumentos reversíveis, dependentes da dose e geralmente leves a moderados na lactato desidrogenase, fosfatase alcalina e ácido úrico foram relatados em 50%, 35%, 25% e 10% dos pacientes tratados com filgrastim nas doses recomendadas, respectivamente. Soro e gama -glutamiltranspeptidase.
Ocasionalmente, também foram relatados aumentos transitórios da pressão arterial, sem necessidade de tratamento clínico.
Desordens vasculares, incluindo doença veno-oclusiva e alterações do volume de fluido, foram ocasionalmente relatadas em pacientes tratados com altas doses de quimioterapia seguida de transplante autólogo de medula óssea. Não foi demonstrada uma relação causal com filgrastim.
Eventos adversos raros de vasculite cutânea foram relatados em pacientes tratados com filgrastim. O mecanismo da vasculite em pacientes tratados com filgrastim não é conhecido.
Casos ocasionais de síndrome de Sweet (dermatose febril aguda) foram descritos. No entanto, como uma porcentagem significativa desses pacientes foi diagnosticada com leucemia, uma condição conhecida por estar associada à síndrome de Sweet, uma relação causal com filgrastim não foi demonstrada.
Em casos individuais, foi relatada uma "exacerbação" da artrite reumatóide.
Têm havido notificações raras de acontecimentos adversos pulmonares, incluindo pneumonia intersticial, edema pulmonar e infiltrações pulmonares com insuficiência respiratória ou síndrome da dificuldade respiratória do adulto (ARDS), que podem ser fatais (ver secção 4.4).
Reações alérgicas: foram relatadas reações do tipo alérgico, incluindo anafilaxia, erupção cutânea, urticária, angioedema, dispneia e hipotensão, ocorrendo em pacientes no primeiro ou subsequente tratamento com filgrastim. Em geral, as notificações foram mais frequentes após a administração. Em alguns casos, os sintomas foram reapareceu após o reinício do tratamento, sugerindo uma relação causal. Em pacientes que apresentem uma reação alérgica grave ao filgrastim, o tratamento deve ser descontinuado definitivamente.
Foram notificados casos isolados de crises de células falciformes em doentes com anemia falciforme ou anemia falciforme (ver secção 4.4). A partir de dados clínicos, a frequência é estimada como incomum.
A pseudogota foi relatada em pacientes com câncer tratados com filgrastim.
Doadores saudáveis submetidos à mobilização de células progenitoras de sangue periférico
Leucocitose (contagem de leucócitos (leucócitos)> 50 x 109 / l) foi relatada em 41% dos doadores e trombocitopenia (plaquetas
Foram notificados aumentos transitórios e ligeiros da fosfatase alcalina, LDH, SGOT e ácido úrico em dadores saudáveis tratados com filgrastim sem sequelas clínicas.
Uma “exacerbação dos sintomas de artrite foi relatada muito raramente.
Reações alérgicas graves foram relatadas muito raramente.
A cefaleia, que se acredita ser desencadeada pelo filgrastim, foi relatada em estudos com doadores saudáveis de PBPC.
Foram notificados casos assintomáticos de esplenomegalia e casos muito raros de ruptura esplénica em dadores saudáveis e em doentes após administração de factores estimuladores de colónias de granulócitos (G-CSFs) (ver secção 4.4).
Os acontecimentos adversos pulmonares em dadores saudáveis (hemoptise, hemorragia pulmonar, infiltrados pulmonares, dispneia e hipoxia) foram notificados muito raramente na experiência pós-comercialização de outros medicamentos filgrastim (ver secção 4.4).
Em pacientes com neutropenia crônica grave (SCN)
As reações adversas relacionadas com a terapêutica com filgrastim foram notificadas em doentes com SCN e, para alguns deles, a sua frequência tende a diminuir ao longo do tempo.
As reações adversas incluem esplenomegalia, que pode ser progressiva em uma minoria de casos, e trombocitopenia. Cefaléia e diarreia foram geralmente relatadas em menos de 10% dos pacientes logo após o início da terapia com filgrastim. Anemia e epistaxe também foram relatadas.
Foram relatados aumentos transitórios no soro sem quaisquer sintomas clínicos para ácido úrico, lactato desidrogenase e fosfatase alcalina. Também foram relatadas quedas transitórias e moderadas na glicose no sangue sem jejum.
Entre as reações adversas provavelmente relacionadas com a terapia com filgrastim que normalmente ocorreram na artralgia, alopecia, osteoporose e erupção cutânea.
Vasculite cutânea foi relatada em 2% dos pacientes com SCN após o uso prolongado. Houve apenas alguns casos de proteinúria / hematúria.
Em pacientes com HIV
A esplenomegalia foi relatada como secundária à terapia com filgrastim no hiperesplenismo e nenhum paciente foi submetido à esplenectomia. A relação com o tratamento com filgrastim é desconhecida, pois a esplenomegalia é comum em pacientes infectados pelo HIV e está presente em vários graus na maioria dos pacientes com AIDS.
População pediátrica
Os dados de ensaios clínicos em doentes pediátricos indicam que a segurança e eficácia do filgrastim são semelhantes em adultos e crianças a receber quimioterapia citotóxica, sugerindo que não existem diferenças relacionadas com a idade na farmacocinética do filgrastim. A única reação adversa notificada de forma consistente foi dor músculo-esquelética, que não difere da experiência na população adulta.
Não há dados suficientes para avaliar melhor o uso de filgrastim em pacientes pediátricos.
Outras populações especiais
Uso geriátrico
Em geral, não foram observadas diferenças na segurança ou eficácia entre indivíduos com mais de 65 anos de idade e adultos jovens (> 18 anos de idade) recebendo quimioterapia citotóxica e a experiência clínica não identificou diferenças nas respostas entre pacientes adultos mais velhos e mais jovens. Não existem dados suficientes para avaliar o uso de filgrastim em indivíduos geriátricos para as outras indicações aprovadas de filgrastim.
Pacientes pediátricos com neutropenia crônica grave (SNG)
Foram notificados casos de diminuição da densidade óssea e osteoporose em doentes pediátricos com neutropenia crónica grave a receber tratamento crónico com filgrastim. A frequência é estimada como "comum" a partir de dados de ensaios clínicos.
Notificação de suspeitas de reações adversas
A notificação de suspeitas de reações adversas ocorridas após a autorização do medicamento é importante porque permite a monitorização contínua da relação benefício / risco do medicamento. Os profissionais de saúde são convidados a notificar quaisquer suspeitas de reações adversas através do sistema nacional de notificação. "Anexo V .
04.9 Overdose
Os efeitos da sobredosagem com filgrastim não foram demonstrados.
A descontinuação da terapia com filgrastim geralmente resulta em uma redução de 50% nos neutrófilos circulantes em 1-2 dias e volta ao normal em 1-7 dias.
05.0 PROPRIEDADES FARMACOLÓGICAS
05.1 Propriedades farmacodinâmicas
Grupo farmacoterapêutico: imunoestimulante, fatores estimuladores de colônias.
Código ATC: L03AA02.
O Nivestim é um medicamento biossimilar. Informação detalhada está disponível no site da Agência Europeia de Medicamentos www.ema.europa.eu
O G-CSF humano é uma glicoproteína que regula a produção e a liberação de neutrófilos funcionais da medula óssea. O Nivestim, que contém r-metHuG-CSF (filgrastim), induz um aumento acentuado na contagem de neutrófilos no sangue periférico e um aumento menos acentuado nos monócitos em 24 horas. Em alguns pacientes com neutropenia crônica grave, o filgrastim pode induzir até mesmo um ligeiro aumento no número de eosinófilos e basófilos circulantes da linha de base; alguns desses pacientes podem apresentar eosinofilia ou basofilia mesmo antes do tratamento. Nas doses recomendadas, o aumento do número de neutrófilos é dependente da dose.Conforme demonstrado nas análises conduzidas, os neutrófilos produzidos em resposta ao filgrastim apresentam propriedades quimiotáticas e fagocíticas normais ou aumentadas. Após a conclusão do tratamento com filgrastim, o número de neutrófilos circulantes diminui em aproximadamente 50% em 1-2 dias e atinge níveis normais em 1-7 dias.
O uso de filgrastim em pacientes submetidos à quimioterapia citotóxica reduz significativamente a incidência, gravidade e duração da nuetropenia e neutropenia febril. O tratamento com filgrastim reduz significativamente a duração da neutropenia febril, uso de antibióticos e hospitalização após quimioterapia de indução na leucemia mieloide aguda ou terapia mieloablativa seguida de transplante de medula óssea. Em ambos os casos, a incidência de febre e infecções documentadas não foi reduzida e a duração da febre não foi reduzida em pacientes submetidos a terapia mieloablativa seguida de transplante de medula óssea.
O uso de filgrastim, sozinho ou após quimioterapia, mobiliza células progenitoras hematopoiéticas para o sangue periférico. Essas células progenitoras de sangue periférico autólogas (PBPCs) podem ser coletadas e reinfundidas após quimioterapia citotóxica de alta dose, como uma alternativa ou em adição ao transplante de medula óssea A infusão de PBPC acelera a recuperação hematopoiética e, portanto, reduz a duração do risco de complicações hemorrágicas e a necessidade de transfusões de trombócitos.
Os receptores de células progenitoras de sangue alogênico periférico mobilizadas com filgrastim, em comparação com os receptores de transplante de medula óssea alogênica, relataram uma recuperação hematológica rápida e significativa com a consequente recuperação significativa de tempo sem fornecimento de trombócitos.
Um estudo europeu retrospectivo, no qual o uso de G-CSF após o transplante alogênico de medula óssea em pacientes com leucemia aguda foi analisado, indicou um risco aumentado de GvHD e mortalidade após a administração de G-CSF (TRM em outro estudo retrospectivo internacional, conduzido com pacientes com leucemias mieloides agudas e crônicas, nenhum efeito sobre o risco de GvHD, TRM e mortalidade foi observado. Em uma meta-análise de estudos de transplante alogênico, incluindo os resultados de nove estudos prospectivos randomizados, 8 estudos retrospectivos e 1 caso-controle estudo, não foram observados efeitos sobre o risco de GvHD agudo, GvHD crônico ou mortalidade relacionada ao tratamento precoce.
a A análise inclui estudos relativos ao transplante de medula óssea no período em questão; GM-CSF foi utilizado em alguns estudos
b A análise inclui pacientes que foram submetidos a transplante de medula óssea durante o período em questão
O uso de filgrastim para mobilização de PBPC em doadores saudáveis antes do transplante de PBPC alogênico resulta na recuperação de 4 x 106 células CD34 + / kg por peso corporal do receptor na maioria dos doadores após duas leucafereses. Doadores normais recebem uma dose de 10 mcg / kg / dia, por via subcutânea, por 4-5 dias consecutivos.
O uso de filgrastim em pacientes, adultos e crianças, com neutropenia crônica grave (neutropenia congênita, cíclica e idiopática grave) induz um aumento acentuado na contagem absoluta de neutrófilos no sangue periférico e uma redução nos episódios infecciosos e eventos relacionados.
O uso de filgrastim em pacientes infectados pelo HIV mantém a contagem de neutrófilos em níveis normais e, portanto, permite que os medicamentos antivirais e / ou mielossupressores sejam administrados conforme o pretendido. Não há evidências de que os pacientes infectados pelo HIV e tratados com filgrastim apresentem aumento da replicação do HIV.
Como foi observado com outros fatores de crescimento hematopoiéticos, o G-CSF também mostra em vitro um efeito estimulante nas células endoteliais humanas.
A eficácia e segurança do Nivestim foram estudadas em estudos de fase III controlados e aleatorizados no cancro da mama.Não foram encontradas diferenças relevantes entre o Nivestim e o medicamento de referência no que diz respeito à duração da neutropenia grave e à incidência de neutropenia febril.
05.2 Propriedades farmacocinéticas
Um ensaio randomizado, não criptografado, de dose única, controlado por comparador, em duplicata crossover conduzido em 46 voluntários saudáveis, mostrou que o perfil farmacocinético do Nivestim foi comparável ao do medicamento de referência após tratamento subcutâneo e intravenoso.
Num outro estudo randomizado, duplo-cego, de dose múltipla, controlado por comparador, duplo cruzado em 50 voluntários saudáveis, mostrou que o perfil farmacocinético de Nivestim era comparável ao do medicamento de referência após tratamento subcutâneo.
A depuração do filgrastim demonstrou seguir a farmacocinética de primeira ordem após tratamento subcutâneo e intravenoso. A meia-vida de eliminação sérica do filgrastim é de aproximadamente 3,5 horas, com uma taxa de eliminação de aproximadamente 0,6 ml / min / kg. A infusão contínua de filgrastim durante um período de 28 dias em pacientes em fase de recuperação do transplante autólogo de medula óssea não mostrou qualquer acúmulo da droga com meia-vida comparável. Portanto, existe uma correlação linear positiva entre a dose e a concentração sérica de filgrastim, independentemente de ser administrado por via intravenosa ou subcutânea. Após a administração subcutânea das doses recomendadas, as concentrações séricas foram mantidas acima de 10 ng / ml durante 8 - 16 horas. O volume de distribuição no sangue é de aproximadamente 150 ml / kg.
05.3 Dados de segurança pré-clínica
O filgrastim foi estudado em estudos de toxicidade de dose repetida com duração até 1 ano, que revelaram alterações atribuíveis aos efeitos farmacológicos esperados, incluindo aumento de leucócitos, hiperplasia da medula óssea mielóide, granulocitopoiese extramedular e aumento do baço.
Essas alterações são reversíveis após a interrupção do tratamento.
Os efeitos do filgrastim no desenvolvimento pré-natal foram estudados em ratos e coelhos. A administração intravenosa (80 microgramas / kg / dia) de filgrastim em coelhos durante o período de organogênese mostrou toxicidade materna e um aumento de abortos espontâneos, perda pós-implantação e diminuição do tamanho médio da ninhada e peso fetal.
Com base nos dados relatados para outro produto de filgrastim, resultados semelhantes foram observados além do "aumento das malformações fetais com uma dose de 100 mcg / kg / dia, uma dose de toxicidade materna correspondente a uma" exposição sistêmica de aproximadamente 50-90. Vezes a exposição observada em pacientes tratados com a dose clínica de 5 mcg / kg / dia. O nível em que nenhum efeito adverso para toxicidade embrio-fetal foi observado neste estudo foi de 10 mcg / kg / dia, o que correspondeu a uma exposição sistêmica de aproximadamente 3-5 vezes a exposição observada em pacientes tratados com a dose clínica.
Em ratas grávidas, nenhuma toxicidade materna ou fetal foi observada com doses acima de 575 mcg / kg / dia. A administração de filgrastim à prole de ratos durante os períodos peri-natal e de lactação mostrou um atraso na diferenciação externa e retardo de crescimento (≥ 20 mcg / kg / dia) e uma taxa de sobrevivência ligeiramente reduzida (100 mcg / kg / dia). Dia) .
Nenhum efeito sobre a fertilidade foi observado em ratos machos ou fêmeas para filgrastim.
06.0 INFORMAÇÕES FARMACÊUTICAS
06.1 Excipientes
Ácido acético, glacial
Hidróxido de sódio
Sorbitol (E420)
Polissorbato 80
Água para injetáveis
06.2 Incompatibilidade
Nivestim não deve ser diluído com soluções de cloreto de sódio.
O filgrastim diluído pode ser absorvido por vidro e plástico, a menos que seja diluído em solução de glicose para perfusão a 50 mg / ml (5%) (ver secção 6.6).
Este medicamento não deve ser misturado com outros medicamentos, exceto os listados na secção 6.6.
06.3 Período de validade
Seringa pré-cheia
30 meses.
Após diluição
A estabilidade química e física da solução diluída para perfusão foi demonstrada durante 24 horas entre 2 ° C e 8 ° C. Do ponto de vista microbiológico, o produto deve ser utilizado imediatamente. Se o medicamento não for usado imediatamente, o usuário é responsável pelo tempo de armazenamento e pelas condições anteriores ao uso; o medicamento pode ser conservado até 24 horas a uma temperatura entre 2 ° C e 8 ° C, a menos que a diluição ocorra em condições assépticas controladas e validadas.
06.4 Precauções especiais para armazenamento
Conservar e transportar refrigerado (2 ° C - 8 ° C).
Não congele.
Manter as seringas pré-cheias na embalagem exterior para protegê-las da luz.
A exposição acidental a temperaturas de congelamento até 24 horas não tem efeitos adversos na estabilidade de Nivestim.A seringa pré-cheia congelada pode ser descongelada e devolvida ao frigorífico para utilização posterior. Se a exposição a baixas temperaturas for superior a 24 horas ou se congelado por mais de uma vez, o Nivestim NÃO deve ser usado mais.
Dentro do seu prazo de validade e para uso ambulatorial, o paciente pode retirar o produto da geladeira e armazená-lo em temperatura ambiente (não acima de 25 ° C) por um período e até 7 dias. Período, o produto não deve mais ser colocado refrigerador e deve ser descartado.
Para condições de conservação do medicamento após diluição, ver secção 6.3.
06.5 Natureza da embalagem primária e conteúdo da embalagem
Seringa pré-cheia (vidro tipo I) com agulha para injeção (aço inoxidável) com proteção de segurança da agulha, contendo 0,2 ml de solução para injeção / perfusão.
Embalagem com 1, 5 ou 10 seringas pré-cheias.
Nem todos os tamanhos de embalagem podem ser comercializados.
06.6 Instruções de uso e manuseio
Se necessário, Nivestim pode ser diluído em solução injetável de glicose a 50 mg / ml (5%).
A diluição para uma concentração final abaixo de 0,2 MU (2 mcg) por ml nunca é recomendada.
A solução deve ser inspecionada visualmente antes do uso.Só devem ser usadas soluções límpidas e sem partículas.
Em pacientes tratados com filgrastim diluído em concentrações abaixo de 1,5 MU (15 mcg) por ml, albumina sérica humana (HSA) deve ser adicionada em uma concentração final de 2 mg / ml.
Exemplo: Em um volume final a ser injetado de 20 ml, doses totais de filgrastim abaixo de 30 MU (300 mcg) devem ser administradas pela adição de 0,2 ml de solução de albumina humana a 20%.
Filgrastim diluído em solução de glicose a 50 mg / ml (5%) é compatível com vidro e muitos plásticos, incluindo PVC, poliolefina (um copolímero de polipropileno e polietileno) e polipropileno.
Nivestim não contém conservantes. Devido ao risco de contaminação bacteriana, as seringas Nivestim destinam-se a uma única utilização. O medicamento não utilizado e os resíduos derivados deste medicamento devem ser eliminados de acordo com a legislação local.
07.0 TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
Hospira UK Limited
Queensway
Royal Leamington Spa
Warwickshire CV31 3RW
Reino Unido
08.0 NÚMERO DE AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
EU / 1/10/631/001
040158014
EU / 1/10/631/002
040158026
EU / 1/10/631/003
040158038
09.0 DATA DA PRIMEIRA AUTORIZAÇÃO OU RENOVAÇÃO DA AUTORIZAÇÃO
Data da primeira autorização: 08 de junho de 2010
10.0 DATA DE REVISÃO DO TEXTO
D.CCE maio de 2015