O que é Glubrava?
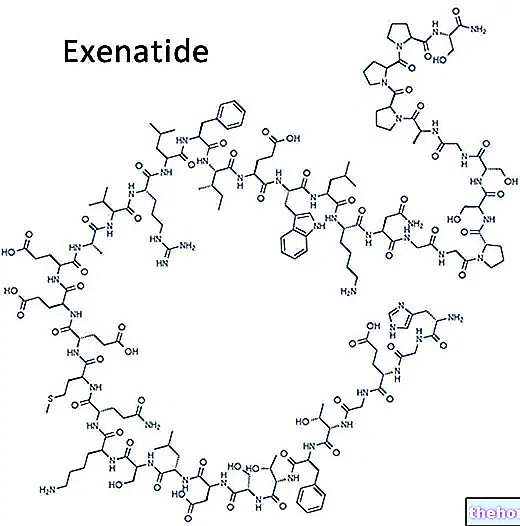
O Glubrava é um medicamento disponível na forma de comprimidos oblongos brancos contendo duas substâncias ativas, pioglitazona (15 mg) e cloridrato de metformina (850 mg).
O medicamento é semelhante ao Competact, já autorizado na União Europeia (UE) A empresa que fabrica o Competact concordou que os seus dados científicos fossem utilizados com o Glubrava.
Para que é utilizado o Glubrava?
O Glubrava é utilizado em doentes (especialmente aqueles com excesso de peso) com diabetes não insulino-dependente (diabetes tipo 2). O Glubrava é utilizado em doentes que não estão suficientemente controlados com metformina em monoterapia (um medicamento antidiabético) em doses máximas.
O medicamento só pode ser obtido mediante receita médica.
Como é usado o Glubrava?
A dose normal de Glubrava consiste em um comprimido tomado duas vezes ao dia. Os doentes que mudam de metformina isolada para Glubrava podem necessitar de introduzir pioglitazona lentamente até ser atingida uma dose de 30 mg por dia. Quando necessário, é possível mudar diretamente da metformina para o Glubrava. Tomar Glubrava com ou logo após as refeições pode reduzir os problemas de estômago causados pela metformina.Em pacientes idosos, a função renal deve ser monitorada regularmente.
Como funciona o Glubrava?
O diabetes tipo 2 é uma doença em que o pâncreas não produz insulina suficiente para controlar o nível de glicose no sangue. O Glubrava contém dois princípios ativos com ação diferente cada: A pioglitazona torna as células (adiposas, musculares e hepáticas) mais sensíveis à insulina, o que permite ao organismo utilizar melhor a insulina que produz. A metformina basicamente inibe a produção de glicose e reduz sua absorção no intestino.O resultado da ação combinada dos dois princípios ativos é a redução da glicose presente no sangue, o que auxilia no controle do diabetes tipo 2.
Como foi estudado o Glubrava?
A pioglitazona isolada foi aprovada pela UE sob o nome de Actos e pode ser usada em conjunto com a metformina no tratamento da diabetes tipo 2 em pacientes nos quais a metformina por si só não fornece controle suficiente. Três estudos realizados com Actos usado em combinação com metformina separadamente comprimidos têm sido usados para apoiar o uso de Glubrava para a mesma indicação. Esses estudos duraram de 4 meses a dois anos e 1.305 pacientes tomaram a dose combinada. Esses estudos mediram a concentração no sangue de uma substância (HbA1c) que dá uma "indicação da eficácia do controle da glicose no sangue".
Qual o benefício demonstrado pelo Glubrava durante os estudos?
Em todos os estudos, a adição de 30 mg de pioglitazona à metformina resultou em melhor controle da glicose no sangue, com os níveis de HbA1c diminuindo ainda mais em 0,64 - 0,89% em comparação com os níveis obtidos apenas com metformina.
Qual é o risco associado ao Glubrava?
Os efeitos colaterais mais comuns de Glubrava (observados em 1 a 10 pacientes em cada 100) são anemia (contagem baixa de glóbulos vermelhos), distúrbios visuais, aumento de peso, artralgia (dor nas articulações), dor de cabeça, hematúria (sangue na urina) e disfunção erétil (dificuldade de ereção). Para a lista completa dos efeitos secundários notificados com o Glubrava, consulte o Folheto Informativo.
O Glubrava não deve ser utilizado em doentes alérgicos à pioglitazona, metformina ou aos outros componentes do medicamento, bem como em doentes com insuficiência cardíaca ou problemas hepáticos ou renais. O Glubrava é contraindicado em pacientes com uma doença que causa falta de oxigênio nos tecidos, como ataque cardíaco ou choque recente. Glubrava não deve ser usado na intoxicação por álcool, cetoacidose diabética (níveis elevados de cetonas), condições que podem afetar os rins e durante a amamentação.Para a lista completa de restrições, consulte o Folheto Informativo.
Por que foi aprovado o Glubrava?
O Comité dos Medicamentos para Uso Humano (CHMP) concluiu que a eficácia da pioglitazona e da metformina na diabetes tipo 2 foi demonstrada e que o Glubrava simplifica o tratamento e melhora a adesão quando é necessária uma combinação das substâncias ativas.
O CHMP concluiu que os benefícios do Glubrava são superiores aos seus riscos para o tratamento da diabetes tipo 2 e concordou em conceder a Autorização de Introdução no Mercado para o Glubrava.
Mais informações sobre o Glubrava
Em 11 de dezembro de 2007, a Comissão Europeia concedeu à Takeda Global Research and Development Centre (Europe) Ltd uma "Autorização de Introdução no Mercado" para o Glubrava, válida em toda a União Europeia.
Para obter a versão completa do EPAR de Glubrava, clique aqui.
Última atualização deste resumo: 03-2008.
As informações sobre Glubrava publicadas nesta página podem estar desatualizadas ou incompletas. Para um uso correto dessas informações, consulte a página Isenção de responsabilidade e informações úteis.