A ligação peptídica é uma ligação covalente que se estabelece entre duas moléculas, quando o grupo carboxila de uma reage com o grupo amino da outra por meio de uma reação de condensação (ou desidratação, que leva - ou seja - à eliminação de uma molécula de água) .
Normalmente, a ligação peptídica é formada entre dois aminoácidos, resultando em um dipeptídeo.
Como um dipeptídeo em sua molécula ainda inclui um grupo amino e um carboxi, ele pode formar uma ligação peptídica com um terceiro aminoácido, dando origem a um tripeptídeo e assim por diante. Quando o número de aminoácidos é relativamente pequeno é denominado oligopeptídeo, enquanto se o número de aminoácidos aumenta é denominado polipeptídeo ou proteína.

Na realidade, apesar da figura, a ligação peptídica não é do tipo simples, mas tem 60% de natureza de ligação simples e 40% de ligação dupla.
Nos organismos vivos, a formação da ligação peptídica é catalisada por uma enzima - chamada peptidil transferase - presente na subunidade principal dos ribossomos.
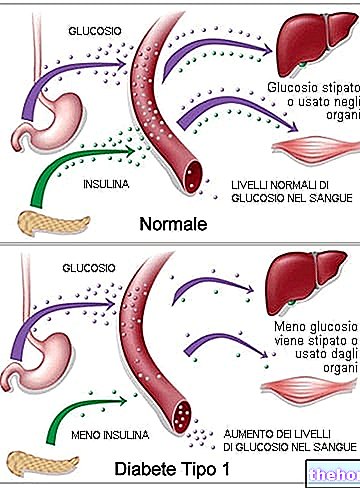
As proteínas introduzidas na dieta também são constituídas por cadeias de aminoácidos unidas por ligações peptídicas. Durante a digestão, essas ligações são quebradas por determinadas enzimas (peptidases) presentes no suco gástrico e pancreático. Os únicos aminoácidos, uma vez absorvidos pelo intestino, passam do sangue e são captados pelas células - especialmente as do fígado - que os unem por meio de novas ligações peptídicas para formar as proteínas de que precisam (não só estruturais, mas também hormonais, enzimáticas , etc. De facto, na natureza existe um grande número de proteínas, com diferentes características físico-químicas, que derivam das diferentes propriedades dos 20 aminoácidos normais e da forma como se combinam na cadeia polipeptídica. Basta pensar que uma proteína de 100 aminoácidos, portanto relativamente pequenos, pode consistir em possíveis cadeias polipeptídicas de 20100 = 1,27 x 10130. As instruções para construir a cadeia de aminoácidos correta estão contidas no genoma do indivíduo.