A análise elementar de proteínas fornece os seguintes valores médios: 55% de carbono, 7% de hidrogênio e 16% de nitrogênio; é claro que as proteínas diferem umas das outras, mas sua composição elementar média difere pouco dos valores indicados acima .
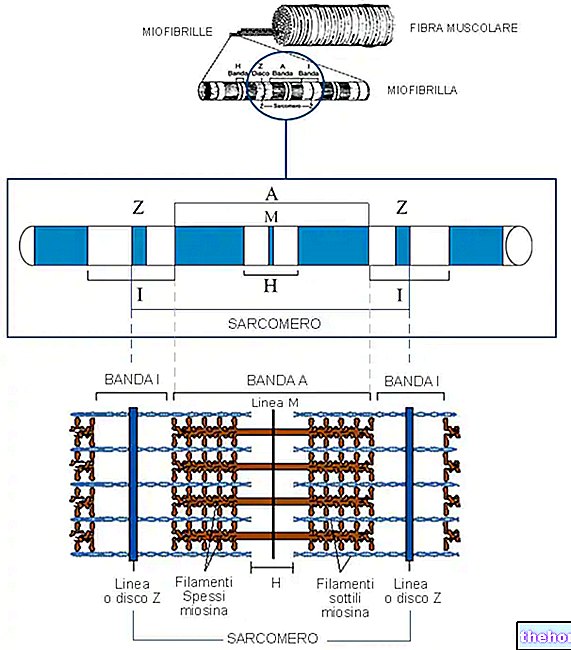
Constitucionalmente, as proteínas são macromoléculas formadas a partir de α-aminoácidos naturais; os aminoácidos unem-se através da ligação amida que é estabelecida pela reação entre um grupo amino de um a-aminoácido e o carboxila de outro a-aminoácido.
Esta ligação (-CO-NH-) também é chamada de ligação peptídica, uma vez que se liga a peptídeos (aminoácidos em combinação):
o obtido é um dipeptídeo porque é composto por dois aminoácidos. Uma vez que um dipeptídeo contém um grupo amino livre em uma extremidade (NH2) e um carboxil na outra (COOH), ele pode reagir com um ou mais aminoácidos e alongar a cadeia tanto da direita quanto da esquerda, com a mesma reação visto acima.
A sequência de reações (que, aliás, não são tão simples assim) pode continuar indefinidamente: até que haja um polímero chamado polipeptídeo ou proteína. A distinção entre peptídeos e proteínas está ligada ao peso molecular: normalmente, para pesos moleculares superiores a 10.000, falamos de proteínas.
Ligar aminoácidos para obter até mesmo proteínas pequenas é uma tarefa difícil, embora recentemente um método automático de produção de proteínas a partir de aminoácidos tenha sido desenvolvido, o que dá excelentes resultados.
A proteína mais simples, portanto, é composta de 2 aminoácidos: por convenção internacional, a numeração ordenada de aminoácidos em uma estrutura de proteína começa a partir do aminoácido com o grupo a-amino livre.
codificação para esta proteína) que encontra dificuldades químicas não negligenciáveis.
Foi possível determinar a seqüência ordenada de aminoácidos por meio da degradação de Edman: a proteína é reagida com o fenilisotiocianato (FITC); inicialmente, o dupleto de nitrogênio α-amino ataca o fenilisotiocianato formando o derivado tiocarbamil; subsequentemente, o produto obtido cicliza dando o derivado de feniltio-hidantoína que é fluorescente.
Edman criou uma máquina chamada sequenciador que ajusta automaticamente os parâmetros (tempo, reagentes, pH, etc.) para degradação e fornece a estrutura primária das proteínas (por isso ele recebeu o Prêmio Nobel).
A estrutura primária não é suficiente para interpretar totalmente as propriedades das moléculas de proteína; acredita-se que essas propriedades dependem, de maneira essencial, da configuração espacial que as moléculas de proteínas tendem a assumir, dobrando-se de várias maneiras: ou seja, assumindo o que foi definido como estrutura secundária das proteínas.
A estrutura secundária das proteínas é oscilante, ou seja, tende a se desintegrar com o aquecimento; então, as proteínas se desnaturam, perdendo muitas de suas propriedades características. Além do aquecimento acima de 70 ° C, a desnaturação também pode ser causada por irradiação ou pela ação de reagentes (de ácidos fortes, por exemplo).
A desnaturação das proteínas devido ao efeito térmico é observada, por exemplo, pelo aquecimento da clara do ovo: ela perde a aparência gelatinosa e se transforma em uma substância branca insolúvel. No entanto, a desnaturação das proteínas leva à destruição de sua estrutura secundária, mas deixa sua estrutura primária inalterada (a concatenação dos vários aminoácidos).
As proteínas assumem a estrutura terciária quando sua cadeia, embora ainda flexível apesar da curvatura da estrutura secundária, se dobra de modo a originar um arranjo tridimensional contorcido em forma de corpo sólido. Responsáveis pela estrutura terciária são sobretudo as ligações dissulfureto que podem ser estabelecidas entre a cisteína -SH espalhada ao longo da molécula.
Já a estrutura quaternária pertence apenas a proteínas formadas por duas ou mais subunidades. A hemoglobina, por exemplo, é composta por dois pares de proteínas (ou seja, em todas as quatro cadeias de proteínas) localizadas nos vértices de um tetraedro de modo a dar origem a uma estrutura esférica; as quatro cadeias de proteínas são mantidas juntas por forças iônicas e ligações não covalentes.
Outro exemplo de estrutura quaternária é a da insulina, que parece ser composta de até seis subunidades de proteínas organizadas em pares nos vértices de um triângulo no centro do qual estão dois átomos de zinco.
Proteínas fibrosas
São proteínas com certa rigidez e com eixo muito mais longo que as outras, a proteína fibrosa presente em maior quantidade na natureza é o colágeno (ou colágeno).
Uma proteína fibrosa pode assumir diferentes estruturas secundárias: α-hélice, β-folha e, no caso do colágeno, tripla hélice; A hélice α é a estrutura mais estável, seguida pela folha β, enquanto a menos estável das três é a hélice tripla.
direito se, seguindo o esqueleto principal (orientado de baixo para cima), é realizado um movimento semelhante ao de um parafuso à direita; enquanto a hélice é de mão esquerda se o movimento for análogo ao aparafusamento de um parafuso do lado esquerdo. Nas hélices α do lado direito, os substituintes -R dos aminoácidos são perpendiculares ao eixo principal da proteína e estão voltados para fora, enquanto no lado esquerdo mão a-hélices os substituintes -R estão voltados para dentro. As a-hélices destras são mais estáveis do que as canhotas porque entre o vati -R c "há menos interação e menos impedimento estérico. Todas as a-hélices encontradas nas proteínas são dextrorotais.
A estrutura da hélice α é estabilizada pelas ligações de hidrogênio (pontes de hidrogênio) que são formadas entre o grupo carboxila (-C = O) de cada aminoácido e o grupo amino (-NH) encontrado quatro resíduos posteriormente no seqüência linear.
Um exemplo de proteína com estrutura em hélice α é a queratina do cabelo.
Ao alongar a estrutura da hélice α, a transição da hélice α para a folha β é realizada; também o calor ou o estresse mecânico permitem passar da hélice α para a estrutura da folha β.
Normalmente, em uma proteína, as estruturas da folha β estão próximas umas das outras porque ligações de hidrogênio entre cadeias podem ser estabelecidas entre porções da própria proteína.
Em proteínas fibrosas, a maior parte da estrutura da proteína é organizada em uma hélice α ou folha β.
Proteínas globulares
Eles têm uma estrutura espacial quase esférica (devido às inúmeras mudanças na direção da cadeia polipeptídica); algumas porções do ser podem ser rastreadas até uma estrutura de hélice α ou folha β e outras porções não são, em vez disso, atribuíveis a essas formas: o arranjo não é aleatório, mas organizado e repetitivo.
As proteínas até agora referidas são substâncias de constituição completamente homogênea: ou seja, sequências puras de aminoácidos combinados; tais proteínas são ditas simples; existem proteínas constituídas por uma parte proteica e uma parte não proteica (grupo da próstata) denominadas proteínas conjugado.
, nas unhas, na córnea e no cristalino do olho, entre os espaços intersticiais de alguns órgãos (por exemplo, o fígado) e assim por diante.
A sua estrutura confere-lhe capacidades mecânicas específicas; tem grande resistência mecânica associada a alta elasticidade (por exemplo, nos tendões) ou alta rigidez (por exemplo, nos ossos) dependendo da função que deve desempenhar.
Uma das propriedades mais curiosas do colágeno é sua simplicidade constitutiva: é composto por cerca de 30% de prolina e cerca de 30% de glicina; os outros 18 aminoácidos só precisam compartilhar os 40% restantes da estrutura da proteína. A sequência de aminoácidos do colágeno é notavelmente regular: para cada três resíduos, o terceiro é glicina.
A prolina é um aminoácido cíclico no qual o grupo R se liga ao nitrogênio α-amino e isso lhe confere certa rigidez.
A estrutura final é uma cadeia repetitiva com a forma de uma "hélice; dentro da cadeia de colágeno, as ligações de hidrogênio estão ausentes. O colágeno é uma "hélice esquerda com um passo (comprimento correspondente a uma volta da hélice) maior do que a" hélice α; a hélice de colágeno é tão frouxa que três cadeias de proteínas são capazes de envolver uma à outra formando um " corda única: estrutura em hélice tripla.
A tripla hélice do colágeno é, no entanto, menos estável do que a α-hélice e a estrutura da folha β.
Vamos agora ver o mecanismo pelo qual o colágeno é produzido; considere, por exemplo, a ruptura de um vaso sanguíneo: essa ruptura é acompanhada por uma miríade de sinais com o objetivo de fechar o vaso, formando assim o coágulo.
A coagulação requer pelo menos trinta enzimas especializadas. Após o coágulo é necessário continuar com a reparação do tecido; células próximas à ferida também produzem colágeno. Para isso, primeiro é induzida a expressão de um gene, ou seja, organismos que a partir da informação de um gene são capazes de produzir a proteína (a informação genética é transcrita no mRNA que sai do núcleo e chega aos ribossomos no citoplasma onde a informação genética é traduzida em proteína). Em seguida, o colágeno é sintetizado nos ribossomos (parece uma hélice esquerda composta por cerca de 1200 aminoácidos e tendo um peso molecular de cerca de 150.000 d) e então se acumula nos lúmens onde torna-se substrato para enzimas capazes de realizar modificações pós-traducionais (modificações da linguagem traduzida por "mRNA); no colágeno, essas modificações consistem na hidroxilação de algumas cadeias laterais, principalmente prolina e lisina.
A falha das enzimas que levam a essas alterações causa o escorbuto: é uma doença que inicialmente causa rompimento dos vasos sanguíneos, rompimento dos dentes que pode ser seguido por hemorragias interintestinais e morte; pode ser causado pelo uso contínuo de alimentos de longa duração.
Posteriormente, devido à ação de outras enzimas, ocorrem outras modificações que consistem na glicosidação dos grupos hidroxila da prolina e da lisina (um açúcar se liga ao oxigênio do OH); essas enzimas são encontradas em outras áreas que não o lúmen, portanto, a proteína, ao sofrer modificações, migra para dentro do retículo endoplasmático para terminar em sacos (vesículas) que se fecham e se desprendem do retículo: dentro delas está contido o pró glicosidado -monômero de colágeno; o último atinge o aparelho de Golgi onde determinadas enzimas reconhecem a cisteína presente na parte do terminal carboxi do pró-colágeno glicosidado e fazem com que as diferentes cadeias se aproximem e formem pontes de dissulfeto: desta forma, três cadeias de Os pró-colágenos glicosidados são obtidos ligados entre si e este é o ponto de partida do qual as três cadeias, interpenetrando-se, então, espontaneamente, dão origem à tripla hélice. As três cadeias de pró-colágeno glicosidado ligadas entre si alcançam, então, uma vesícula que, sufocando-se, desprende-se do aparelho de Golgi, transportando as três cadeias para a periferia da célula onde, através do fus íon com a membrana plasmática, o trimeter é expelido da célula.
No espaço extracelular, existem enzimas particulares, as pró-colágeno peptidases, que removem da espécie expelida da célula, três fragmentos (um para cada hélice) de 300 aminoácidos l "um, da parte terminal do carboxi e três fragmentos (um para cada hélice) de cerca de 100 aminoácidos cada, da parte aminoterminal: permanece uma hélice tripla consistindo de cerca de 800 aminoácidos por hélice conhecida como tropocolágeno.
O tropocolágeno tem a aparência de uma haste bastante rígida; os diferentes trímeros se associam a ligações covalentes para dar estruturas maiores: o microfibrilas. Nas microfibrilas, os vários trímeros estão dispostos de forma escalonada; muitas microfibrilas constituem feixes de tropocolágeno.
Nos ossos, entre as fibras de colágeno, existem espaços intersticiais nos quais se depositam sulfatos e fosfatos de cálcio e magnésio: esses sais também cobrem todas as fibras; isso torna os ossos rígidos.
Nos tendões, os espaços intersticiais são menos ricos em cristais do que nos ossos, enquanto proteínas menores estão presentes do que no tropocolágeno: isso dá elasticidade aos tendões.
A osteoporose é uma doença causada pela falta de cálcio e magnésio que impossibilita a fixação de sais nas áreas intersticiais das fibras do tropocolágeno.