Ingredientes ativos: Fingolimod
GILENYA 0,5 mg cápsulas duras
Por que Gilenya é usado? Para que serve?
O que é Gilenya
O ingrediente ativo do Gilenya é fingolimod.
Para que serve Gilenya
Gilenya é usado em adultos para o tratamento da esclerose múltipla (EM) recorrente-remitente, particularmente em:
Pacientes que não responderam à terapia com tratamento para EM.
ou
Pacientes com EM grave de evolução rápida.
Gilenya não cura a esclerose múltipla, mas ajuda a reduzir o número de recidivas e a retardar a progressão da deficiência física causada pela esclerose múltipla.
O que é esclerose múltipla
A EM é uma doença crônica que afeta o sistema nervoso central (SNC), que inclui o cérebro e a medula espinhal. Na EM, a inflamação destrói a bainha protetora (chamada mielina) que reveste os nervos no SNC e impede que os nervos funcionem como deveriam. Esse processo é chamado de desmielinização.
A EM recorrente-remitente é caracterizada por ataques recorrentes (recidivas) de sintomas neurológicos que refletem um estado inflamatório do sistema nervoso central. Os sintomas variam de paciente para paciente, mas geralmente envolvem dificuldade para andar, dormência, visão ou distúrbios do equilíbrio. Os sintomas de recidiva podem desaparecer completamente quando a recaída passa, mas algumas queixas podem persistir.
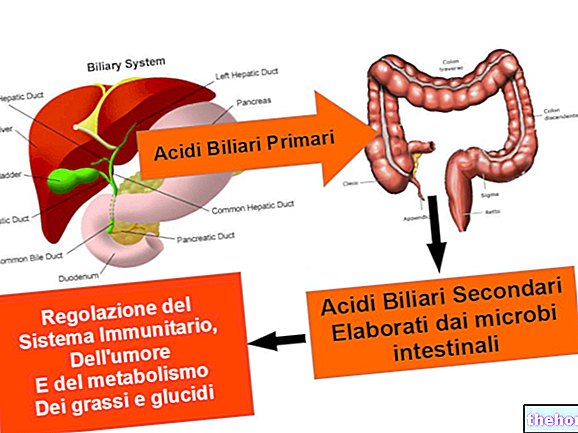
Como funciona Gilenya
Gilenya ajuda a proteger o sistema nervoso de ataques do sistema imunológico, reduzindo a capacidade de alguns glóbulos brancos (linfócitos) de circularem livremente no corpo e evitando que alcancem o cérebro e a medula espinhal. Isso limita os danos aos nervos causados pela EM.
Contra-indicações Quando Gilenya não deve ser usado
Não tome Gilenya
- se tem uma resposta imunitária reduzida (devido a uma síndrome de imunodeficiência, uma doença ou medicamentos que deprimem o sistema imunitário).
- se tem uma infecção grave em curso ou uma infecção crónica em curso, como hepatite ou tuberculose.
- se você tem câncer ativo (exceto se for um tipo de câncer de pele chamado câncer de pele de células basais).
- se tem problemas graves de fígado.
- se tem alergia ao fingolimod ou a qualquer outro componente deste medicamento.
Se algum destes se aplicar a si, informe o seu médico antes de tomar Gilenya.
Precauções de uso O que você precisa saber antes de tomar Gilenya
Fale com o seu médico antes de tomar Gilenya:
- se tem batimento cardíaco irregular e anormal.
- se sentir sintomas de frequência cardíaca baixa (por exemplo, tonturas, náuseas ou palpitações).
- se tem problemas cardíacos, bloqueio dos vasos sanguíneos do coração, se teve um ataque cardíaco ou paragem cardíaca no passado ou se tem angina.
- se já teve um AVC no passado.
- se sofre de insuficiência cardíaca.
- se tem problemas respiratórios graves durante o sono (apneia do sono grave).
- se foi informado de que tem um EKG anormal.
- se está a tomar ou tomou recentemente medicamentos para o batimento cardíaco irregular, como quinidina, disopiramida, amiodarona ou sotalol.
- se está a tomar ou tomou recentemente medicamentos que diminuem os batimentos cardíacos (tais como bloqueadores beta, verapamilo, diltiazem ou ivabradina, digoxina, medicamentos anticolinesterásicos ou pilocarpina).
- se já teve episódios de perda súbita de consciência ou desmaios (síncope).
- se você pretende ser vacinado.
- se você nunca teve catapora.
- se você tem ou teve distúrbios visuais ou outros sinais de inchaço na área de visão central (mácula) na parte posterior do olho (uma condição conhecida como edema macular, veja abaixo), se você tem ou teve uma "inflamação ou" infecção do olho (uveíte) ou se você tem diabetes (que pode causar problemas nos olhos).
- se tem problemas de fígado.
- se tem pressão arterial elevada que não pode ser controlada por medicamentos.
- se tiver problemas pulmonares graves ou se tiver tosse por fumar.
Se algum destes se aplicar a si, informe o seu médico antes de tomar Gilenya.
Batimento cardíaco lento (bradicardia) e batimento cardíaco irregular: No início do tratamento, Gilenya causa um abrandamento do ritmo cardíaco. Como resultado, pode sentir tonturas ou cansaço, percepção dos batimentos cardíacos ou uma queda da pressão arterial. Se estes efeitos forem pronunciados , contacte o seu médico, uma vez que pode necessitar de tratamento imediato. Gilenya também pode causar um batimento cardíaco irregular, especialmente após a primeira dose. O batimento cardíaco irregular normalmente volta ao normal em menos de um dia. O ritmo cardíaco lento normalmente volta. ao normal dentro de um mês. .
O seu médico irá pedir-lhe para ficar na clínica ou hospital durante pelo menos 6 horas após a administração da primeira dose de Gilenya, durante a qual o seu pulso e pressão arterial serão medidos a qualquer momento: desta forma, podem ser tomadas medidas adequadas, caso de efeitos secundários que ocorrem no início do tratamento. Deve ter um eletrocardiograma disponível antes da primeira dose de Gilenya e no final das 6 horas de monitorização. O seu médico pode verificar o seu eletrocardiograma continuamente durante este período. Se após 6 horas sua frequência cardíaca está muito baixa ou diminui, ou se seu EKG mostrar anormalidades, você pode precisar ser observado por um período mais longo (pelo menos mais 2 horas e possivelmente até a manhã seguinte), até que esses problemas sejam resolvidos. O mesmo pode acontecer se ela tomar G de novo ilenya após uma interrupção do tratamento, dependendo da duração da interrupção e durante quanto tempo está a tomar Gilenya antes da interrupção.
Se tem ou corre o risco de ter batimento cardíaco irregular ou anormal, se o seu EKG estiver anormal ou se tiver doença cardíaca ou insuficiência cardíaca, Gilenya pode não ser adequado para si.
Se alguma vez teve episódios de perda súbita de consciência ou diminuição da frequência cardíaca, Gilenya pode não ser adequado para si. Será visto por um cardiologista (especialista em coração) que o aconselhará sobre como iniciar o seu tratamento com Gilenya, incluindo monitorização até à manhã seguinte.
Se estiver a tomar medicamentos que podem causar uma diminuição da frequência cardíaca, Gilenya pode não ser adequado para si. Será visto por um cardiologista que irá avaliar se pode tomar medicamentos que não diminuem a sua frequência cardíaca como alternativa, permitindo-lhe iniciar o tratamento com Gilenya. Se esta mudança na terapia não for possível, o seu cardiologista irá aconselhá-lo sobre como iniciar o tratamento com Gilenya, incluindo monitoramento até a manhã seguinte.
Se você nunca teve catapora: Se você nunca teve catapora, o seu médico verificará sua imunidade contra o vírus que a causa (vírus da varicela zoster). Se não está protegido contra o vírus, pode necessitar de uma vacinação antes de iniciar o tratamento com Gilenya. Se isso ocorrer, o seu médico irá adiar o início do tratamento com Gilenya por até um mês após completar o esquema de vacinação completo.
Infecções: Gilenya reduz o número de glóbulos brancos (especialmente linfócitos). Os glóbulos brancos combatem as infecções. Enquanto estiver a tomar Gilenya (e até 2 meses após interromper o tratamento), pode ter infecções mais facilmente. Qualquer infecção existente pode piorar. As infecções podem ser graves e fatais. Se você acha que tem uma infecção, febre, sintomas de gripe ou dor de cabeça acompanhada de torcicolo, sensibilidade à luz, náusea e / ou confusão (podem ser sintomas de meningite), entre em contato com o seu médico imediatamente.
Edema macular: antes de iniciar o tratamento com Gilenya, se você tem ou teve distúrbios visuais ou outros sinais de inchaço na área de visão central (mácula) na parte posterior do olho, se você tem ou teve uma "inflamação ou" infecção ocular (uveíte) ou se tiver diabetes, o seu médico pode pedir-lhe para fazer um exame aos olhos.
O seu médico pode pedir-lhe para fazer um exame oftalmológico 3-4 meses após o início do tratamento com Gilenya.
A mácula é uma pequena área da retina localizada na parte posterior do olho que permite ver formas, cores e detalhes de forma clara e nítida. Gilenya pode causar inchaço da mácula, uma condição conhecida como edema macular. ocorre inchaço, geralmente nos primeiros 4 meses de tratamento com Gilenya.
O edema macular é mais provável de ocorrer se você tem diabetes ou teve uma "inflamação do olho" chamada uveíte. Nestes casos, o seu médico irá querer examiná-lo regularmente para detetar os primeiros sinais de edema macular.
Se já sofreu de edema macular, fale com o seu médico antes de reiniciar o tratamento com Gilenya.
O edema macular pode causar alguns dos sintomas visuais (neurite óptica) que também ocorrem durante os ataques de esclerose múltipla. Na fase inicial, pode não haver sintomas. Informe o seu médico sobre quaisquer alterações na visão. O seu médico pode pedir que você os consulte . submeter-se a um exame oftalmológico, especialmente se:
- a área de visualização central está fora de foco ou tem sombras;
- um ponto cego se desenvolve na área de visão central;
- têm dificuldade em distinguir cores ou detalhes finos.
Testes da função hepática: Se tiver problemas hepáticos graves, não deve tomar Gilenya. O tratamento com Gilenya pode afetar a função hepática. Você provavelmente não notará nenhum sintoma, mas se notar amarelecimento da pele ou da parte branca dos olhos, urina escura anormal ou náuseas e vômitos inexplicáveis, informe o seu médico imediatamente.
Se tiver algum destes sintomas após iniciar o tratamento com Gilenya, informe o seu médico imediatamente.
Durante os primeiros doze meses de tratamento, o seu médico irá pedir-lhe para fazer análises ao sangue para verificar a sua função hepática. Se os resultados indicarem que existe um problema de fígado, pode ser necessário interromper o tratamento com Gilenya.
Alta pressão
Uma vez que Gilenya provoca um ligeiro aumento da tensão arterial, o seu médico pode pedir-lhe regularmente uma verificação da tensão arterial. Problemas pulmonares Gilenya tem um efeito fraco na função pulmonar. Os efeitos indesejáveis podem ocorrer mais facilmente em doentes com problemas pulmonares graves ou tosse por fumar.
Hemograma O efeito desejado do tratamento com Gilenya é a redução da quantidade de glóbulos brancos no sangue. Normalmente, estes voltam ao normal 2 meses após a interrupção do tratamento. Se precisar de fazer análises ao sangue, informe o seu médico que está a tomar Gilenya .
Antes de iniciar o tratamento com Gilenya, o seu médico irá confirmar se a sua contagem de glóbulos brancos é suficiente e pode pedir-lhe para repetir a contagem regularmente. Se não tiver glóbulos brancos suficientes, pode ser necessário interromper o tratamento com Gilenya.
Síndrome de encefalopatia reversível posterior (PRES)
Uma síndrome chamada encefalopatia reversível posterior (PRES) foi raramente relatada em pacientes com esclerose múltipla tratados com Gilenya. Os sintomas podem incluir início repentino de forte dor de cabeça, confusão, convulsões e alterações na visão. Informe o seu médico se algum destes sintomas ocorrer durante o tratamento com Gilenya.
Uso em idosos
A experiência com Gilenya em doentes idosos com idade superior a 65 anos é limitada.Se ainda tiver dúvidas, fale com o seu médico.
Crianças e adolescentes
Gilenya não se destina a ser utilizado em crianças e adolescentes com menos de 18 anos de idade, uma vez que não foi estudado em doentes com EM com menos de 18 anos.
Interações Quais medicamentos ou alimentos podem alterar o efeito de Gilenya
Informe o seu médico ou farmacêutico se estiver a tomar ou tiver tomado recentemente, ou se vier a tomar outros medicamentos. Informe o seu médico se você estiver tomando algum dos seguintes medicamentos:
- Medicamentos que suprimem ou modificam o sistema imunológico, incluindo outros medicamentos usados para tratar a EM, como interferão beta, acetato de glatirâmero, natalizumab, mitoxantrona, teriflunomida, fumarato de dimetilo ou alemtuzumab. Não deve utilizar Gilenya com estes medicamentos porque podem intensificar o efeito no sistema imunitário (ver também “Não tome Gilenya”).
- Corticosteróides, devido ao possível efeito aditivo no sistema imunológico.
- Vacinas. Se precisar de ser vacinado, consulte primeiro o seu médico. Durante e até 2 meses após o tratamento com Gilenya, você não deve receber alguns tipos de vacinas (vacinas vivas atenuadas), pois podem desencadear a infecção que deveriam prevenir. Outras vacinas podem não funcionar tão bem como de costume se administradas neste momento .
- Medicamentos que diminuem os batimentos cardíacos (como beta-bloqueadores, como atenolol). O uso concomitante de Gilenya com estes medicamentos pode intensificar o efeito na frequência cardíaca nos primeiros dias de tratamento com Gilenya.
- Medicamentos para batimento cardíaco irregular, como quinidina, disopiramida, amiodarona ou sotalol. O seu médico pode decidir não prescrever Gilenya se estiver a tomar estes tipos de medicamentos, pois podem intensificar o efeito no batimento cardíaco irregular.
- Outros medicamentos:
- inibidores de protease, anti-infecciosos como cetoconazol, antifúngicos azólicos, claritromicina ou telitromicina.
- carbamazepina, rifampicina, fenobarbital, fenitoína, efavirenz ou erva de São João (risco potencial de eficácia reduzida).
Avisos É importante saber que:
Gravidez e amamentação
Antes de iniciar o tratamento com Gilenya, o seu médico pode pedir-lhe para fazer um teste de gravidez para se certificar de que não está grávida. Enquanto estiver a tomar Gilenya ou durante dois meses após interromper o tratamento, deve evitar engravidar porque existe o risco de prejudicar o bebé. Fale com o seu médico sobre métodos contraceptivos fiáveis a utilizar durante o tratamento. Com Gilenya e 2 meses após interromper o tratamento. .
Se engravidar enquanto está a tomar Gilenya, pare o tratamento e informe o seu médico imediatamente. O seu médico decidirá consigo o que é melhor para si e para o seu bebé.
Não amamente enquanto estiver a tomar Gilenya. Gilenya é excretado no leite materno com risco de efeitos colaterais graves para o recém-nascido.
Consulte o seu médico ou farmacêutico antes de tomar qualquer medicamento.
Condução e utilização de máquinas
O seu médico dir-lhe-á se a sua doença lhe permite conduzir e utilizar máquinas com segurança. Não se espera que Gilenya afete a capacidade de conduzir e utilizar máquinas.
No entanto, no início do tratamento terá de permanecer no consultório médico ou hospital durante 6 horas após a administração da primeira dose de Gilenya. A capacidade de conduzir e utilizar máquinas pode ficar comprometida durante este período e potencialmente depois.
Dosagem e método de uso Como usar Gilenya: Dosagem
O tratamento com Gilenya será supervisionado por um médico com experiência no tratamento da esclerose múltipla.
Tome este medicamento sempre de acordo com as indicações do seu médico.
Em caso de dúvida, consulte seu médico. A dose é uma cápsula uma vez ao dia. Tome Gilenya uma vez ao dia com um copo de água.Gilenya pode ser tomado com ou sem alimentos.
Tomar Gilenya à mesma hora todos os dias irá ajudá-lo a lembrar-se de quando deve tomar o medicamento.
Não exceda a dose recomendada.
O seu médico pode mudar diretamente do tratamento com interferão beta, acetato de glatirâmero ou fumarato de dimetilo para Gilenya se não houver sinais de anomalias causadas pelo tratamento anterior. Seu médico pode solicitar que você faça um exame de sangue para descartar essas anormalidades. Após interromper o natalizumab, pode ser necessário esperar 2-3 meses antes de iniciar o tratamento com Gilenya. Para mudar de teriflunomida, o seu médico pode aconselhá-lo a esperar um determinado período de tempo ou a prosseguir com um procedimento de eliminação acelerada. Se você foi tratado com alemtuzumab, é necessária uma avaliação cuidadosa e uma discussão com seu médico para decidir se Gilenya é adequado para você.
Se não tem a certeza de quanto tempo irá tomar Gilenya, pergunte ao seu médico ou farmacêutico.
Overdose O que fazer se você tiver tomado Gilenya demais
Se você tomar mais Gilenya do que deveria
Se tomou demasiadas cápsulas de Gilenya, informe o seu médico imediatamente.
Se você esquecer de tomar Gilenya
Se está a tomar Gilenya há menos de 1 mês e se esqueceu de tomar 1 dose durante o dia inteiro, fale com o seu médico antes de tomar a próxima dose. O seu médico pode decidir observá-lo quando tomar a próxima dose.
Se está a tomar Gilenya há pelo menos 1 mês e se esqueceu de tomar o medicamento há mais de 2 semanas, fale com o seu médico antes de tomar a próxima dose. O seu médico pode decidir observá-lo quando tomar a próxima dose.No entanto, se se esqueceu de tomar o seu medicamento durante 2 semanas ou menos, pode tomar a próxima dose conforme planeado.
Nunca tome uma dose dupla para compensar uma dose esquecida.
Se você parar de tomar Gilenya
Não pare de tomar Gilenya nem altere a sua dose sem primeiro falar com o seu médico.
Gilenya permanecerá no corpo até 2 meses após a interrupção do tratamento. O número de glóbulos brancos (linfócitos) pode permanecer baixo durante este período e os efeitos secundários descritos neste folheto podem ainda ocorrer. Após interromper o tratamento com Gilenya, pode ser necessário esperar de 6 a 8 semanas antes de iniciar um novo tratamento para esclerose múltipla.
Se necessitar de reiniciar Gilenya após mais de 2 semanas de interrupção do tratamento, o efeito na frequência cardíaca que normalmente ocorre no início do tratamento pode ocorrer novamente hospital em observação Não reinicie Gilenya após interromper o tratamento por mais de duas semanas sem consultar o seu doutor.
Caso ainda tenha dúvidas sobre o uso deste medicamento, fale com o seu médico ou farmacêutico
Efeitos colaterais Quais são os efeitos colaterais do Gilenya
Como todos os medicamentos, este medicamento pode causar efeitos colaterais, embora nem todas as pessoas os tenham.
Alguns efeitos colaterais podem ser ou se tornar graves
Frequentes (podem afetar até 1 em 10 pessoas):
- Tosse com catarro, desconforto no peito, febre (sinais de doenças pulmonares)
- Infecção pelo vírus do herpes (fogo de Santo Antônio ou herpes zoster), com sintomas como bolhas, queimação, coceira ou dor na pele, geralmente na parte superior do corpo ou no rosto. Outros sintomas podem ser febre e fraqueza nos estágios iniciais . infecção, seguida por dormência, coceira ou manchas vermelhas com dor intensa
- Batimento cardíaco lento (bradicardia), ritmo cardíaco irregular
Pouco frequentes (podem afetar até 1 em 100 pessoas):
- Pneumonia com sintomas como febre, tosse, dificuldade em respirar
- Edema macular (inchaço na área de visão central da retina na parte posterior do olho) com sintomas como sombras ou pontos cegos no centro da visão, visão turva, problemas para distinguir cores ou detalhes
Raros (podem afetar até 1 em 1000 pessoas):
- Síndrome chamada encefalopatia reversível posterior. Os sintomas podem incluir início súbito de dor de cabeça intensa, confusão, convulsões e / ou distúrbios visuais
Casos isolados:
- Infecções criptocócicas (um tipo de infecção fúngica), incluindo meningite criptocócica com sintomas como dor de cabeça acompanhada de rigidez do pescoço, sensibilidade à luz, náusea e / ou confusão.
Se sentir algum destes efeitos secundários, informe o seu médico imediatamente.
Outros efeitos colaterais
Muito comuns (podem afetar mais de 1 em 10 pessoas):
- Infecção pelo vírus da gripe com sintomas como fadiga, calafrios, dor de garganta, dores nas articulações ou musculares, febre
- Sensação de pressão ou dor nas bochechas e na testa (sinusite)
- Dor de cabeça
- Diarréia
- Dor nas costas
- Exames de sangue mostrando níveis mais elevados de enzimas hepáticas
- Tosse
Frequentes (podem afetar até 1 em 10 pessoas):
- Micose, uma "infecção fúngica da pele (pitiríase versicolor)
- Tontura
- Dor de cabeça intensa, muitas vezes acompanhada por náuseas, vômitos e sensibilidade à luz (enxaqueca)
- Níveis baixos de glóbulos brancos (linfócitos, leucócitos)
- Fraqueza
- Erupção cutânea com coceira, vermelhidão e queimação (eczema)
- Coceira
- Níveis aumentados de gorduras (triglicerídeos) no sangue
- Perda de cabelo
- Respiração ofegante
- Depressão
- Visão turva (ver também a seção sobre "edema macular" Alguns efeitos colaterais podem ser ou tornar-se graves ")
- Hipertensão (Gilenya pode causar um ligeiro aumento da pressão arterial)
Pouco frequentes (podem afetar até 1 em 100 pessoas):
- Níveis baixos de alguns glóbulos brancos (neutrófilos)
- Humor deprimido
Raros (podem afetar até 1 em 1000 pessoas):
- Distúrbios dos vasos sanguíneos
- Distúrbios do sistema nervoso
- Câncer do sistema linfático (linfoma)
Desconhecido (a frequência não pode ser estimada a partir dos dados disponíveis):
- Reação alérgica e erupção cutânea
Se algum destes efeitos secundários ocorrer de forma grave, informe o seu médico.
Relatório de efeitos colaterais
Se tiver quaisquer efeitos secundários, fale com o seu médico ou farmacêutico, incluindo quaisquer efeitos secundários possíveis não mencionados neste folheto. Você também pode relatar os efeitos colaterais diretamente através do sistema nacional de notificação listado no Apêndice V. Ao relatar os efeitos colaterais, você pode ajudar a fornecer mais informações sobre a segurança deste medicamento.
Expiração e retenção
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após o prazo de validade impresso na embalagem exterior e no blister após “VAL” / “VAL”. A data de validade refere-se ao último dia desse mês.
Não armazene acima de 25ºC.
Conservar na embalagem original para proteger o medicamento da umidade.
Não use embalagens danificadas ou com sinais de adulteração.
Não deite quaisquer medicamentos na canalização ou no lixo doméstico. Pergunte ao seu farmacêutico como deitar fora os medicamentos que já não utiliza. Isto ajudará a proteger o ambiente.
O que Gilenya contém
- O ingrediente ativo é fingolimod. Cada cápsula contém 0,5 mg de fingolimod (como cloridrato).
- Os outros ingredientes são: Conteúdo da cápsula: estearato de magnésio, manitol Invólucro da cápsula: óxido de ferro amarelo (E172), dióxido de titânio (E171), gelatina Tinta: laca (E904), álcool desidratado, álcool isopropílico, álcool butílico, propilenoglicol, água purificada , solução de amônia concentrada, hidróxido de potássio, óxido de ferro preto (E172), óxido de ferro amarelo (E172), dióxido de titânio (E171), dimeticona
Descrição da aparência de Gilenya e conteúdo da embalagem
As cápsulas de Gilenya 0,5 mg têm um corpo opaco branco opaco e uma cabeça opaca amarelo escuro. A inscrição "FTY0,5mg" em preto está gravada na cabeça e duas faixas amarelas estão gravadas no corpo.
Gilenya está disponível em embalagens de 7, 28 ou 98 cápsulas ou em embalagens múltiplas de 84 cápsulas (3 embalagens de 28 cápsulas). Nem todos os tamanhos de embalagem podem ser comercializados.
Folheto Informativo Fonte: AIFA (Agência Italiana de Medicamentos). Conteúdo publicado em janeiro de 2016. As informações apresentadas podem não estar atualizadas.
Para ter acesso à versão mais atualizada, é aconselhável acessar o site da AIFA (Agência Italiana de Medicamentos). Isenção de responsabilidade e informações úteis.
01.0 NOME DO MEDICAMENTO
CÁPSULAS DURAS GILENYA 0,5 MG
▼ Medicamento sujeito a monitorização adicional. Isso permitirá a rápida identificação de novas informações de segurança. Os profissionais de saúde são solicitados a notificar quaisquer suspeitas de reações adversas. Consulte a seção 4.8 para obter informações sobre como notificar reações adversas.
02.0 COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Cada cápsula contém 0,5 mg de fingolimod (como cloridrato).
Para a lista completa de excipientes, consulte a seção 6.1.
03.0 FORMA FARMACÊUTICA
Cápsula dura.
Cápsula de 16 mm com capa opaca amarela intensa e corpo opaco branco; gravura “FTY0,5 mg” a preto na cabeça e duas bandas circulares amarelas gravadas no corpo.
04.0 INFORMAÇÕES CLÍNICAS
04.1 Indicações terapêuticas
Gilenya é indicado isoladamente, como um medicamento modificador da doença, na esclerose múltipla recorrente-remitente altamente ativa nos seguintes grupos de pacientes adultos:
- Pacientes com alta atividade da doença, apesar do tratamento com pelo menos uma terapia modificador de doença (consulte as seções 4.4 e 5.1 para exceções e informações sobre esmaecimento).
Esses pacientes podem ser definidos como aqueles que não responderam a um curso de terapia completo e adequado (geralmente pelo menos um ano de tratamento) com pelo menos uma terapia modificador de doença. Os pacientes devem ter tido pelo menos 1 recidiva no ano anterior durante a terapia e ter pelo menos 9 lesões T2 hiperintensas na ressonância magnética cerebral ou pelo menos 1 lesão que realça o gadolínio. Um paciente não respondedor também pode ser definido como um paciente que tem uma taxa de recaída inalterada ou aumentada em comparação com o ano anterior ou que tem recaídas graves.
ou
- Pacientes com esclerose múltipla recorrente-remitente grave de evolução rápida, definida por duas ou mais recidivas incapacitantes em um ano, e com 1 ou mais lesões que aumentam o gadolínio na ressonância magnética cerebral ou com um aumento significativo na carga de lesões T2 em comparação com uma ressonância magnética anterior recentemente realizado.
04.2 Posologia e método de administração
O tratamento deve ser iniciado e supervisionado por um médico com experiência em esclerose múltipla.
Dosagem
A dose recomendada de Gilenya é uma cápsula de 0,5 mg por via oral uma vez ao dia. Gilenya pode ser tomado durante e fora das refeições.
Recomenda-se realizar a mesma monitorização que no início do tratamento após a primeira dose se o tratamento for interrompido por:
• 1 ou mais dias durante as primeiras duas semanas de tratamento
• mais de 7 dias durante a terceira e quarta semanas de tratamento
• mais de 2 semanas após um mês de tratamento.
Se a interrupção do tratamento for de duração mais curta do que o descrito acima, o tratamento deve continuar com a administração da próxima dose conforme planeado (ver secção 4.4).
Populações especiais
Cidadãos idosos
Gilenya deve ser utilizado com precaução em doentes com idade igual ou superior a 65 anos uma vez que os dados de segurança e eficácia disponíveis são insuficientes (ver secção 5.2).
Função renal prejudicada
Nos principais estudos essenciais realizados na esclerose múltipla, Gilenya não foi estudado em doentes com compromisso da função renal. Com base em estudos de farmacologia clínica, nenhum ajuste de dose é necessário em pacientes com insuficiência renal leve a grave.
Função hepática prejudicada
Gilenya não deve ser utilizado em doentes com compromisso hepático grave (Child-Pugh classe C) (ver secção 4.3). Embora não seja necessário ajuste da dose em doentes com compromisso hepático ligeiro ou moderado, recomenda-se precaução ao iniciar o tratamento nestes doentes (ver secções 4.4 e 5.2).
Pacientes diabéticos
Gilenya não foi estudado em pacientes com esclerose múltipla e diabetes mellitus. Gilenya deve ser utilizado com precaução nestes doentes devido a um possível aumento do risco de edema macular (ver secções 4.4 e 4.8). Esses pacientes devem ser submetidos a exames oftalmológicos regulares para detectar sinais de edema macular.
População pediátrica
A segurança e eficácia de Gilenya em crianças com 0-18 anos de idade não foram ainda estabelecidas Os dados atualmente disponíveis estão descritos na secção 5.2, mas não pode ser feita nenhuma recomendação sobre a posologia.
04.3 Contra-indicações
- Síndrome de imunodeficiência diagnosticada.
- Pacientes com risco aumentado de infecções oportunistas, incluindo pacientes imunocomprometidos (incluindo aqueles tratados com terapias imunossupressoras concomitantes ou imunocomprometidos por terapias anteriores).
- Infecções ativas graves, infecções ativas crônicas (hepatite, tuberculose).
- Tumores malignos ativos diagnosticados, com exceção de pacientes com câncer de pele basocelular.
- Insuficiência hepática grave (classe C de Child-Pugh).
- Hipersensibilidade à substância ativa ou a qualquer um dos excipientes listados na secção 6.1.
04.4 Advertências especiais e precauções adequadas de uso
Bradiarritmia
O início do tratamento com Gilenya resulta numa diminuição transitória da frequência cardíaca e pode também estar associada a atrasos na condução atrioventricular, incluindo episódios isolados de bloqueio atrioventricular completo, transitório e de resolução espontânea (ver secções 4.8 e 5.1).
Após a administração da primeira dose, a diminuição da frequência cardíaca começa dentro de uma hora e é máxima nas primeiras 6 horas. Nos dias seguintes, esse efeito pós-dose persiste, embora geralmente em menor intensidade, e geralmente diminui nas semanas seguintes .. Com a dosagem continuada, a frequência cardíaca média retorna à linha de base dentro de um mês. No entanto, em determinados pacientes, a frequência cardíaca pode não retornar à linha de base no final do primeiro mês. Anormalidades de condução geralmente são transitórias e assintomáticas. Geralmente não é necessário tratamento e resolvido nas primeiras 24 horas após o início do tratamento. Se necessário, a diminuição da freqüência cardíaca induzida por fingolimod pode ser revertida pela administração parenteral de doses de atropina ou isoprenalina.
Todos os pacientes devem fazer um eletrocardiograma e medição da pressão arterial antes da primeira dose de Gilenya e após 6 horas. Todos os pacientes devem ser monitorados por 6 horas quanto a sinais e sintomas de bradicardia, com medição de frequência cardíaca e pressão arterial de hora em hora.Monitorização contínua (em tempo real) de ECG é recomendada durante essas 6 horas.
Se ocorrerem sintomas de bradiarritmia após a administração, procedimentos adequados de gestão clínica do paciente devem ser iniciados e o monitoramento continuado até que os sintomas tenham remitido. Se um paciente necessitar de intervenção farmacológica durante o monitoramento após a primeira dose, o monitoramento deve ser feito até a manhã seguinte em um ambiente hospitalar e deve ser repetido após a segunda dose de Gilenya.
Se, ao final de 6 horas, o valor da frequência cardíaca for o mais baixo após a primeira dose (sugerindo que o efeito farmacodinâmico máximo no coração pode ainda não se manifestar), o monitoramento deve ser continuado por pelo menos 2 horas e até o coração a frequência aumenta novamente. Monitoramento adicional também é necessário (pelo menos até a manhã seguinte e em qualquer caso até que os sintomas sejam resolvidos) se, após 6 horas da administração da primeira dose, a frequência cardíaca for batimentos por minuto, ou se o o eletrocardiograma mostra novo início de bloqueio atrioventricular de segundo grau ou superior, ou se o intervalo QTc for ≥500 mseg. O início de bloqueio atrioventricular de terceiro grau a qualquer momento também deve levar a uma extensão da monitoração (pelo menos até a manhã seguinte).
Devido ao risco de distúrbios graves do ritmo, Gilenya não deve ser usado em pacientes com bloqueio atrioventricular de segundo grau Mobitz tipo II ou superior, em pacientes com síndrome do seio doente ou bloqueio sinoatrial, história de bradicardia sintomática ou síncope recorrente, ou em pacientes com prolongamento QT significativo (QTc> 470 mseg (mulheres) ou> 450 mseg (homens)). Como a bradicardia significativa pode ser mal tolerada em pacientes com doença cardíaca isquêmica conhecida (incluindo angina pectoris), doença cerebrovascular, história de infarto do miocárdio, insuficiência cardíaca congestiva, história de parada cardíaca, hipertensão não controlada ou apneia do sono grave, Gilenya não deve ser usado em esses pacientes. O tratamento com Gilenya só deve ser considerado nesses pacientes se os benefícios esperados superarem os riscos potenciais; se for decidido iniciar a terapia com Gilenya, um cardiologista deve ser consultado antes de iniciar o tratamento para definir o monitoramento mais adequado. A monitorização é recomendada pelo menos até à manhã seguinte para o início do tratamento (ver também secção 4.5).
Gilenya não foi estudado em pacientes com arritmias que requerem tratamento com antiarrítmicos de classe Ia (por exemplo, quinidina, disopiramida) ou classe III (por exemplo, amiodarona, sotalol).Os antiarrítmicos das classes Ia e III foram associados a casos de torsades de pointes em pacientes com bradicardia. Uma vez que o início do tratamento com Gilenya resulta numa diminuição da frequência cardíaca, Gilenya não deve ser utilizado concomitantemente com estes medicamentos.
Experiência com Gilenya em pacientes em tratamento concomitante com beta-bloqueadores, bloqueadores dos canais de cálcio que causam uma diminuição na freqüência cardíaca (como verapamil, diltiazem ou ivabradina), ou com outros medicamentos que podem diminuir a freqüência cardíaca (por exemplo, digoxina, drogas anticolinesterásicas ou pilocarpina Uma vez que o início do tratamento com Gilenya também está associado a uma diminuição da frequência cardíaca (ver também secção 4.8 Bradiarritmia), a utilização concomitante destes medicamentos no início do tratamento com Gilenya pode estar associada a bradicardia grave e bloqueio cardíaco. Devido aos potenciais efeitos aditivos na frequência cardíaca, o tratamento com Gilenya não deve ser iniciado em doentes a receber estes medicamentos (ver também secção 4.5). Nestes doentes, o tratamento com Gilenya só deve ser considerado se os benefícios esperados ultrapassarem os riscos potenciais. Se a terapia com Gilenya for considerada, recomenda-se que um cardiologista seja consultado antes de iniciar o tratamento, para considerar a mudança para outros medicamentos que não causem uma diminuição da frequência cardíaca. Se não for possível interromper o tratamento com estes medicamentos, um cardiologista deve ser consultado para definir a monitorização adequada no início do tratamento.Recomenda-se a monitorização pelo menos até à manhã seguinte (ver também secção 4.5).
Dependendo da duração da interrupção e da duração do tratamento (tempo entre o início do tratamento e a sua descontinuação), os efeitos na frequência cardíaca e na condução atrioventricular podem reaparecer quando o tratamento com Gilenya é reiniciado. Recomenda-se realizar a mesma monitorização que no início do tratamento após a primeira dose se o tratamento for interrompido por:
• 1 ou mais dias durante as primeiras duas semanas de tratamento
• mais de 7 dias durante a terceira e quarta semanas de tratamento
• mais de 2 semanas após um mês de tratamento.
Se a interrupção do tratamento for de duração mais curta do que o descrito acima, o tratamento deve continuar com a administração da próxima dose conforme planeado.
Intervalo QT
Em um estudo completo do intervalo QT conduzido com doses de fingolimode de 1,25 mg ou 2,5 mg, no estado estacionário (quando o efeito cronotrópico negativo do fingolimode ainda estava presente), o tratamento com fingolimode induziu o prolongamento da dose. Intervalo QT corrigido (QTc), com o limite superior do intervalo de confiança de 90% ≤ 13,0 ms. Nenhuma correlação dose-resposta ou exposição-resposta foi observada entre fingolimod e o prolongamento do intervalo QTc., Nem como um valor absoluto, nem como uma mudança em relação ao valor basal.
O significado clínico destes resultados é desconhecido. Nenhum prolongamento clinicamente significativo do intervalo QT foi observado em estudos em pacientes com esclerose múltipla, mas os pacientes em risco de desenvolver prolongamento do intervalo QT não foram incluídos nos ensaios clínicos.
Os medicamentos que podem prolongar o intervalo QTc devem ser evitados em pacientes com fatores de risco significativos, como hipocalemia ou prolongamento congênito do intervalo QT.
Infecções
Um efeito farmacodinâmico relevante de Gilenya é a redução dependente da dose nas contagens de linfócitos periféricos para 20-30% dos valores basais. Isto deve-se ao sequestro reversível de linfócitos em tecidos linfóides (ver secção 5.1).
Um hemograma completo recente (isto é, feito 6 meses antes ou depois de interromper a terapia anterior) deve estar disponível antes do início do tratamento com Gilenya. Também é recomendado durante o tratamento para avaliar hemogramas periodicamente após 3 meses e pelo menos anualmente a partir de então, e em caso de início de sinais de infecção. Uma contagem absoluta de linfócitos inferior a 0,2x109 / l, se confirmada, deve levar à descontinuação. tratamento até o retorno ao normal, uma vez que fingolimod foi descontinuado em ensaios clínicos em pacientes com contagens absolutas de linfócitos abaixo de 0,2x109 / l.
O início do tratamento com Gilenya deve ser adiado em pacientes com infecções graves em curso até a recuperação.
Os pacientes devem ser avaliados quanto ao seu estado de imunidade para varicela antes de iniciar o tratamento com Gilenya. Na ausência de uma história confirmada pelo médico de varicela ou evidência de um esquema de vacinação contra varicela completo, recomenda-se que os pacientes sejam testados para anticorpos do vírus da varicela-zóster (VZV) antes de iniciar a terapia com Gilenya. Para os doentes com título de anticorpos negativo, é recomendado um esquema de vacinação completo contra a varicela antes de iniciar o tratamento com Gilenya (ver secção 4.8). O início do tratamento com Gilenya deve ser adiado por 1 mês para que a vacinação seja totalmente eficaz.
Os efeitos de Gilenya no sistema imunitário podem aumentar o risco de infecções (ver secção 4.8). Estratégias diagnósticas e terapêuticas eficazes devem ser implementadas em pacientes tratados com Gilenya que apresentam sintomas de infecções. Os pacientes devem ser instruídos a relatar os sintomas de infecção ao médico durante o tratamento com Gilenya.
Se uma infecção grave se desenvolver em um paciente, a descontinuação da terapia com Gilenya deve ser considerada e a relação risco-benefício deve ser avaliada antes de retomar o tratamento.
A eliminação de fingolimod após a descontinuação da terapia pode levar até dois meses e, portanto, o controle da infecção deve ser mantido durante este período. Os pacientes devem ser instruídos a relatar sintomas de infecção dentro de dois meses após a interrupção do fingolimod.
Edema macular
Edema macular com ou sem distúrbios visuais foi relatado em 0,5% dos pacientes tratados com 0,5 mg de fingolimode, principalmente nos primeiros 3-4 meses de terapia (ver seção 4.8). Uma avaliação oftalmológica é, portanto, recomendada 3-4 meses após o início do tratamento. Se os pacientes relatarem distúrbios visuais a qualquer momento durante o tratamento, um exame de fundo de olho, incluindo a mácula, deve ser realizado.
Os doentes com história de uveíte e os doentes com diabetes mellitus apresentam um risco aumentado de desenvolver edema macular (ver secção 4.8). Gilenya não foi estudado em doentes com esclerose múltipla e diabetes mellitus concomitante. Recomenda-se que os pacientes com esclerose múltipla e diabetes mellitus concomitante ou com histórico de uveíte sejam submetidos a uma avaliação oftalmológica antes de iniciar a terapia e verificações de acompanhamento durante o tratamento.
A continuação do tratamento com Gilenya em doentes com edema macular não foi estudada. Recomenda-se que o tratamento com Gilenya seja interrompido se ocorrer edema macular em um paciente. Ao decidir se a terapia com Gilenya deve ou não ser retomada após a recuperação, os benefícios e riscos potenciais para o paciente individual devem ser considerados.
Função do fígado
Foram notificados aumentos das enzimas hepáticas, particularmente alanina aminotransferase (ALT), mas também gama glutamiltranspeptidase (GGT) e aspartato transaminase (AST) em doentes com esclerose múltipla tratados com Gilenya. Em ensaios clínicos, aumentos de ALT ≥3 vezes o limite superior do intervalo normal (LSN) ocorreram em 8,0% dos doentes tratados com fingolimode 0,5 mg em comparação com 1,9% dos doentes tratados com placebo. Aumentos de 5 vezes o limite superior do intervalo normal ocorreu em 1,8% dos doentes tratados com fingolimode e em 0,9% dos doentes tratados com placebo.Em ensaios clínicos, o tratamento com fingolimode foi interrompido se o aumento fosse> 5 vezes o limite superior do intervalo normal. Em alguns pacientes que foram tratados novamente após a descontinuação, as elevações das transaminases hepáticas ocorreram novamente, confirmando uma relação entre esse aumento e o medicamento. Em estudos clínicos, as elevações das transaminases hepáticas ocorreram em qualquer momento durante o tratamento, embora a maioria tenha ocorrido nos primeiros 12 meses. Os níveis de transaminases no sangue voltaram ao normal aproximadamente 2 meses após a interrupção do fingolimod.
Gilenya não foi estudado em doentes com compromisso hepático grave preexistente (Child-Pugh classe C) e, por conseguinte, não deve ser utilizado nestes doentes (ver secção 4.3).
Devido às propriedades imunossupressoras do fingolimod, o início do tratamento deve ser adiado em pacientes com hepatite viral ativa até a resolução da fase ativa.
Análises recentes (ou seja, nos 6 meses anteriores) dos níveis de transaminase e bilirrubina devem estar disponíveis antes do início do tratamento com Gilenya. Na ausência de sintomas clínicos, os níveis de transaminase hepática devem ser verificados após 1, 3, 6, 9 e 12 meses de tratamento e periodicamente depois disso. Se os níveis de transaminase hepática atingirem valores maiores que 5 vezes o limite normal (LSN), verificações mais frequentes devem ser organizadas, incluindo verificações de bilirrubina sérica e fosfatase alcalina (ALP). Se após verificações repetidas, o fígado os valores das transaminases permanecem mais de 5 vezes o limite do normal (LSN), o tratamento com Gilenya deve ser interrompido e reiniciado apenas quando os valores das transaminases do fígado voltaram ao normal.
Em pacientes que apresentam sintomas de disfunção hepática, como náuseas inexplicáveis, vômitos, dor abdominal, fadiga, anorexia, icterícia e / ou urina escura, os níveis das enzimas hepáticas devem ser avaliados; se for confirmada lesão hepática significativa (por exemplo, níveis de transaminase hepática excedendo o limite superior da faixa normal em mais de 5 vezes e / ou aumentos nos níveis de bilirrubina sérica), o tratamento com Gilenya deve ser interrompido. A retomada da terapia dependerá da identificação ou não de outra causa de lesão hepática e do benefício do paciente em retomar a terapia versus o risco de recorrência de disfunção hepática.
Embora não existam dados que demonstrem que os doentes com doença hepática pré-existente têm um risco aumentado de desenvolver testes de função hepática elevados, deve ter-se cuidado ao administrar Gilenya a doentes com história de doença hepática significativa.
Interferência com ensaios sorológicos
Uma vez que fingolimod reduz a contagem de linfócitos sanguíneos redistribuindo-os para órgãos linfóides secundários, não pode ser utilizado para avaliar o estado dos linfócitos de um doente tratado com Gilenya. Os exames laboratoriais que envolvem o uso de células mononucleares circulantes requerem volumes sanguíneos maiores devido à redução do número de linfócitos circulantes.
Efeitos na pressão sanguínea
Os doentes com hipertensão não controlada por medicamento foram excluídos dos ensaios clínicos realizados antes da comercialização do Gilenya; portanto, atenção especial é recomendada se os pacientes com hipertensão não controlada forem tratados com Gilenya.
Em estudos clínicos em pacientes com esclerose múltipla, o tratamento com fingolimode 0,5 mg foi associado a um aumento médio de aproximadamente 3 mmHg na pressão arterial sistólica e aproximadamente 1 mmHg na pressão arterial diastólica: esses aumentos ocorreram aproximadamente 1 mês depois. Início do tratamento e persistiu com tratamento contínuo Num estudo de dois anos controlado com placebo, a hipertensão foi notificada como um acontecimento adverso em 6,5% dos doentes tratados com Gilenya 0,5 mg e em 3,3% dos doentes tratados com placebo. Portanto, a sua pressão arterial deve ser verificada regularmente durante o tratamento com Gilenya.
Efeitos no sistema respiratório
Durante o tratamento com Gilenya, observaram-se ligeiras diminuições dose-dependentes no volume expiratório forçado (FEV1) e na capacidade de difusão do monóxido de carbono (Dlco), diminuições que ocorreram no primeiro mês e permaneceram estáveis ao longo do tratamento. Gilenya deve ser usado com precaução em doentes com doenças respiratórias graves, fibrose pulmonar e doença pulmonar obstrutiva crónica (ver secção 4.8).
Síndrome de encefalopatia reversível posterior
Casos raros de síndrome de encefalopatia reversível posterior (PRES) foram relatados em ensaios clínicos e experiência pós-comercialização com a dose de 0,5 mg (ver seção 4.8). Os sintomas relatados incluíram início súbito de dor de cabeça intensa, náuseas, vômitos, estado mental alterado, visual distúrbios e convulsões. Os sintomas de PRES são geralmente reversíveis, mas podem progredir para acidente vascular cerebral isquêmico ou hemorragia cerebral. Atraso no diagnóstico e no tratamento pode levar a consequências neurológicas permanentes. Se houver suspeita de presença. de PRES, o tratamento com Gilenya deve ser interrompido.
Tratamento prévio com terapias imunossupressoras ou imunomoduladoras
Não foram realizados estudos para avaliar a eficácia e segurança de Gilenya quando os doentes mudam de teriflunomida, fumarato de dimetilo ou alemtuzumab para Gilenya. Quando os doentes mudam de outra terapêutica. modificador de doença em Gilenya, a meia-vida e o mecanismo de ação da outra terapia devem ser levados em consideração para evitar um efeito aditivo no sistema imunológico e, ao mesmo tempo, minimizar o risco de reativação da doença. tratamento com Gilenya para garantir que os efeitos no sistema imunitário induzidos pela terapêutica anterior (por exemplo, citopenia) foram resolvidos.
O tratamento com Gilenya geralmente pode ser iniciado imediatamente após a interrupção da terapia com interferon ou acetato de glatirâmero.
No caso do fumarato de dimetila, o período de esmaecimento deve ser suficiente para restaurar contagens sanguíneas adequadas antes de iniciar o tratamento com Gilenya.
Devido à longa meia-vida do natalizumabe, a eliminação geralmente leva 2 a 3 meses após a interrupção do tratamento. A teriflumonida também é eliminada lentamente do plasma. Sem um procedimento de eliminação acelerado, a depuração da teriflunomida do plasma pode levar de vários meses a 2 anos. Recomenda-se a realização de um procedimento de eliminação acelerada conforme descrito no resumo das características do medicamento para a teriflunomida ou, alternativamente, o período de eliminação não deve ser inferior a 3,5 meses. Deve-se ter cuidado ao trocar os pacientes da terapia com natalizumabe ou teriflunomida para Gilenya em relação aos potenciais efeitos concomitantes no sistema imunológico.
Alemtuzumab tem efeitos imunossupressores intensos e prolongados. Como a verdadeira duração destes efeitos é desconhecida, é recomendado não iniciar o tratamento com Gilenya após alemtuzumab, a menos que os benefícios do tratamento para o paciente individual superem claramente os riscos.
A decisão de co-administrar tratamentos prolongados com corticosteroides deve ser tomada após consideração cuidadosa.
Administração concomitante com potentes indutores do CYP450
Fingolimod deve ser usado com precaução em combinação com indutores potentes do CYP450. Recomenda-se não administrar hipericão concomitantemente (ver secção 4.5).
Descontinuação da terapia
Com base na meia-vida do medicamento, se for tomada a decisão de interromper o tratamento com Gilenya, deve-se deixar um intervalo de 6 semanas sem terapia para permitir que o fingolimod seja eliminado do sangue (ver seção 5.2). A contagem de linfócitos progressivamente retorna aos valores normais 1-2 meses após a descontinuação da terapêutica (ver secção 5.1). Iniciar outras terapias durante este intervalo de tempo resulta na exposição concomitante ao fingolimod. O uso de medicamentos imunossupressores logo após a interrupção da administração de Gilenya pode ter um efeito adicional no sistema imunológico e, portanto, recomenda-se cautela.
04.5 Interações com outros medicamentos e outras formas de interação
Terapias antineoplásicas, imunomoduladoras ou imunossupressoras
As terapêuticas antineoplásicas, imunomoduladoras ou imunossupressoras não devem ser administradas concomitantemente devido ao risco de efeitos aditivos no sistema imunitário (ver secções 4.3 e 4.4).
Também se deve ter cuidado quando os doentes iniciam a terapêutica com Gilenya após a descontinuação do tratamento com terapêuticas de ação prolongada com efeitos no sistema imunitário, tais como natalizumab ou mitoxantrona (ver secção 4.4). de corticosteroides não foi associado a um aumento da taxa de infecções.
Vacinas
A vacinação pode ser menos eficaz durante o tratamento e até dois meses após a interrupção do tratamento com Gilenya.O uso de vacinas vivas atenuadas pode representar um risco de infecções e deve, portanto, ser evitado (ver secções 4.4 e 4.8).
Substâncias que induzem bradicardia
Fingolimod foi estudado em combinação com atenolol e diltiazem.Quando fingolimod foi administrado com atenolol num estudo de interação em voluntários saudáveis, ocorreu uma redução adicional de 15% na frequência cardíaca no início do tratamento; este efeito não foi observado com diltiazem. Devido ao potencial efeito aditivo. Frequência cardíaca, o tratamento com Gilenya não deve ser iniciado em pacientes tomando beta-bloqueadores ou outros medicamentos que podem diminuir a frequência cardíaca, como antiarrítmicos de classe Ia e III, bloqueadores dos canais de cálcio (como ivabradina, verapamil ou diltiazem), digoxina, anticolinesterásicos ou pilocarpina (ver seções 4.4 e 4.8) Se o tratamento com Gilenya for considerado para esses pacientes, um cardiologista deve ser consultado para considerar a troca para outros medicamentos que não causem diminuição da freqüência cardíaca ou para definir uma monitorização adequada no início do tratamento. Se não for possível interromper o tratamento com medicamentos que diminuem a frequência cardíaca, recomenda-se o monitoramento pelo menos até a manhã seguinte.
Mudanças na farmacocinética do fingolimod induzidas por outras substâncias
O fingolimod é metabolizado principalmente pelo CYP4F2. Outras enzimas como o CYP3A4 também podem estar envolvidas na sua metabolização, particularmente no caso de indução potente do CYP3A4. Não se espera que os inibidores potentes das proteínas transportadoras afetem o comportamento do fingolimod. A co-administração de fingolimode com cetoconazol resultou em um aumento de 1,7 vezes na exposição (AUC) a fingolimode e fosfato de fingolimode via inibição de CYP4F2. Deve-se ter cuidado ao administrar fingolimode com substâncias que podem inibir CYP3A4 (inibidores da protease, antifúngicos azólicos, alguns macrolídeos como claritromicina ou telitromicina).
A administração concomitante de carbamazepina 600 mg duas vezes ao dia, atingiu o estado estacionário, e uma dose única de fingolimode 2 mg reduziu a AUC de fingolimode e seu metabólito em aproximadamente 40%. Outros indutores potentes da enzima CYP3A4, como rifampicina, fenobarbital, fenitoína, O efavirenz e a erva de São João podem induzir uma redução na AUC do fingolimod e seu metabólito em pelo menos esta magnitude. Uma vez que pode comprometer a sua eficácia, deve-se ter cuidado ao administrar em combinação, mas a administração concomitante com erva de São João não é recomendada (ver secção 4.4).
Mudanças na farmacologia de outras substâncias induzidas por fingolimod
É improvável que o fingolimod interaja com substâncias metabolizadas principalmente pelas enzimas CYP450 ou substratos das principais proteínas transportadoras.
A coadministração de fingolimode com ciclosporina não resultou em qualquer alteração na exposição à ciclosporina ou fingolimode.Por conseguinte, não se espera que fingolimode altere a farmacocinética de medicamentos que são substratos do CYP3A4.
A coadministração de fingolimod com contraceptivos orais (etinilestradiol e levonorgestrel) não resultou em qualquer alteração na exposição aos contraceptivos orais. Não foram realizados estudos de interação com contraceptivos orais contendo progestogênios; no entanto, não é esperado um efeito do fingolimode sobre a exposição ao progestogênio. a tais drogas.
04.6 Gravidez e lactação
Mulheres com potencial para engravidar / Contracepção em mulheres
Antes de iniciar o tratamento com Gilenya, as mulheres com potencial para engravidar devem ser informadas dos possíveis riscos graves para o feto e da necessidade de utilizar métodos contraceptivos eficazes durante o tratamento com Gilenya. Uma vez que demora cerca de dois meses após a interrupção do tratamento para eliminar o fingolimod do corpo (ver secção 4.4), pode existir o risco potencial para o feto e, portanto, as medidas contraceptivas devem continuar durante esse período.
Gravidez
Um teste de gravidez negativo deve estar disponível antes de iniciar o tratamento em mulheres com potencial para engravidar. As mulheres não devem engravidar durante o tratamento e recomenda-se uma contracepção eficaz. Se uma mulher engravidar durante o tratamento com Gilenya, recomenda-se a descontinuação do tratamento.
Estudos em animais demonstraram toxicidade reprodutiva, incluindo perda fetal e defeitos em órgãos, particularmente tronco arterial persistente e defeito do septo ventricular (ver secção 5.3) .O receptor sobre o qual o fingolimod atua (esfingosina 1-fosfato) está envolvido na formação vascular durante a embriogénese. Existem dados muito limitados sobre a utilização de fingolimod em mulheres grávidas.
Não existem dados sobre os efeitos do fingolimod no trabalho de parto e no parto.
Hora da alimentação
O fingolimode é excretado no leite de animais tratados durante a lactação em concentrações 2 a 3 vezes superiores às encontradas no plasma da mãe (ver secção 5.3). Devido ao potencial para reações adversas graves ao fingolimode em lactentes, mulheres em tratamento com Gilenya não deve amamentar.
Fertilidade
Os dados de estudos pré-clínicos não indicam que fingolimod esteja associado a um risco aumentado de diminuição da fertilidade (ver secção 5.3).
04.7 Efeitos sobre a capacidade de dirigir e usar máquinas
Gilenya não tem ou tem uma influência negligenciável sobre a capacidade de conduzir ou utilizar máquinas.
No entanto, por vezes podem ocorrer tonturas ou sonolência após o início do tratamento com Gilenya Recomenda-se que os doentes sejam observados durante 6 horas ao iniciar o tratamento com Gilenya (ver secção 4.4 Bradiarritmia).
04.8 Efeitos indesejáveis
Resumo do perfil de segurança
A população de segurança de Gilenya é derivada de dois ensaios clínicos de fase III controlados por placebo e um ensaio clínico de fase III de controle ativo conduzido em pacientes com esclerose múltipla recorrente-remitente. Inclui um total de 2.431 pacientes tratados com Gilenya (0,5 ou 1,25 mg). No estudo clínico controlado por placebo de 2 anos D2301 (FREEDOMS), 854 pacientes (placebo: 418 pacientes) foram tratados com fingolimod. No estudo de 2 anos, controlado por placebo, D2309 (FREEDOMS II), 728 pacientes com esclerose múltipla (placebo: 355 pacientes) foram tratados com fingolimod. Os resultados combinados destes dois estudos indicam que as reações adversas mais graves que ocorreram com Gilenya 0,5 mg foram infecções, edema macular e bloqueio atrioventricular transitório no início do tratamento. As reações adversas mais frequentes (incidência ≥ 10%) que ocorreram com Gilenya 0,5 mg foram gripe, sinusite, dor de cabeça, diarreia, dor nas costas, enzimas hepáticas elevadas e tosse. A reação adversa mais frequente com Gilenya 0,5 mg que conduziu à "descontinuação do tratamento foi" níveis elevados de ALT no sangue (2,2%). No estudo de 1 ano D2302 (TRANSFORMS) envolvendo 849 pacientes tratados com fingolimod e usando interferon beta-1α como controle, as reações adversas que ocorreram foram geralmente semelhantes às dos estudos controlados com placebo, levando em consideração a diferente duração do estudo.
As reações adversas notificadas para Gilenya 0,5 mg nos estudos D2301 (FREEDOMS) e D2309 (FREEDOMS II) estão listadas abaixo. As categorias de frequência são definidas usando a seguinte convenção: muito comum (≥1 / 10); comum (≥1 / 100,
Tabela de resumo de reações adversas
* Não relatado nos estudos FREEDOMS, FREEDOMS II e TRANSFORMS. A categorização da frequência de eventos foi baseada em uma estimativa de "exposição ao fingolimod de aproximadamente 10.000 pacientes em todos os ensaios clínicos".
Descrição de algumas reações adversas específicas
Infecções
Em ensaios clínicos em doentes com esclerose múltipla, a taxa global de infecções (65,1%) notificada com a dose de 0,5 mg foi semelhante à observada com placebo. No entanto, as infecções do trato respiratório inferior, principalmente bronquite e, em menor grau, infecções herpéticas e pneumonia, foram mais frequentes em doentes tratados com Gilenya.
Alguns casos de infecção herpética disseminada, incluindo casos fatais, foram relatados mesmo com a dose de 0,5 mg.
Edema macular
Em estudos clínicos em pacientes com esclerose múltipla, o edema macular ocorreu em 0,5% dos pacientes tratados com a dose recomendada de 0,5 mg e em 1,1% dos pacientes tratados com a dose mais elevada (1,25 mg). A maioria dos casos ocorreu nos primeiros 3-4 meses de terapia. Alguns pacientes relataram visão turva e diminuição da acuidade visual; outros eram assintomáticos e o diagnóstico foi feito durante uma consulta oftalmológica de rotina. O edema macular geralmente melhorou ou resolveu espontaneamente após a descontinuação do tratamento. O risco de recorrência após a reexposição ao tratamento não foi estudado .
A incidência de edema macular é aumentada em pacientes com esclerose múltipla com história de uveíte (17% com história de uveíte vs. 0,6% sem história de uveíte). Gilenya não foi estudado em pacientes com esclerose múltipla e diabetes mellitus. doença associada a um risco aumentado de edema macular (ver secção 4.4) .Em estudos clínicos em doentes com transplante renal, incluindo doentes com diabetes mellitus, o tratamento com fingolimode 2,5 mg e 5 mg resultou num aumento duas vezes da incidência de edema macular.
Bradiarritmia
O início do tratamento com Gilenya resulta numa diminuição transitória da frequência cardíaca e também pode estar associada a atrasos na condução atrioventricular. Em ensaios clínicos em doentes com esclerose múltipla, a diminuição máxima da frequência cardíaca foi observada nas primeiras 6 horas após a cirurgia. " início do tratamento, com diminuição da frequência em uma média de 12-13 batimentos por minuto durante o tratamento com Gilenya 0,5 mg. Foi raramente observada uma diminuição da frequência cardíaca abaixo de 40 batimentos por minuto em doentes tratados com Gilenya 0,5 mg. A frequência cardíaca média voltou ao valor basal no prazo de 1 mês após a continuação do tratamento. A bradicardia foi geralmente assintomática, mas alguns doentes apresentaram sintomas ligeiros a moderados, incluindo hipotensão, tonturas, fadiga e / ou palpitações, que desapareceram nas primeiras 24 horas após o início do tratamento (ver também secções 4.4 e 5.1).
Em estudos clínicos em pacientes com esclerose múltipla, bloqueio atrioventricular de primeiro grau (prolongamento do intervalo PR ao ECG) foi observado em 4,7% dos pacientes tratados com fingolimode 0,5 mg, em 2,8% dos pacientes. Pacientes tratados com interferon beta-1α intramuscular e em 1,6% dos pacientes tratados com placebo. O bloqueio atrioventricular de segundo grau foi relatado em menos de 0,2% dos pacientes tratados com Gilenya 0,5 mg. Na experiência pós-comercialização, episódios isolados de bloqueio atrioventricular total transitório, com resolução espontânea completa foram relatados durante 6 horas de monitoramento após a primeira dose de Gilenya. Experiência pós-comercialização, foram geralmente transitórios, assintomáticos e resolvidos nos primeiros 24 Embora nenhuma intervenção médica tenha sido necessária para a maioria dos pacientes, um paciente em tratamento com Gilenya 0,5 mg recebeu isoprenalina após um episódio assintomático de bloqueio atrioventricular tipo 1 Mobitz de segundo grau.
Na experiência pós-comercialização, eventos isolados com início tardio, incluindo assistolia transitória e morte inexplicada, ocorreram dentro de 24 horas após a administração da primeira dose. A avaliação desses casos é complicada pela presença de medicamentos concomitantes e / ou condições pré-existentes A correlação desses eventos com Gilenya é incerta.
Pressão sanguínea
Em estudos clínicos em pacientes com esclerose múltipla, o tratamento com Gilenya 0,5 mg foi associado a um aumento médio da pressão arterial sistólica de aproximadamente 3 mmHg e da pressão arterial diastólica de aproximadamente 1 mmHg: esses aumentos ocorreram aproximadamente 1 mês depois do início do tratamento e foram mantidos com tratamento continuado. Hipertensão foi relatada em 6,5% dos pacientes tratados com fingolimode 0,5 mg e em 3,3% dos pacientes tratados com placebo. Foram relatados casos de hipertensão que podem requerer tratamento com medicamentos anti-hipertensivos ou a descontinuação de Gilenya no primeiro mês em diante no primeiro dia de tratamento (ver também secção 4.4 Efeitos sobre a pressão arterial).
Função do fígado
Foram notificados aumentos das enzimas hepáticas em doentes com esclerose múltipla tratados com Gilenya. Em estudos clínicos, foi observada elevação assintomática dos níveis sangüíneos de ALT ≥3 vezes e ≥5 vezes o limite superior do intervalo normal (LSN) em 8,0% e 1,8% dos pacientes tratados com Gilenya, respectivamente. 0,5 mg. Em alguns pacientes re- tratamento após a descontinuação, ocorreram novamente elevações das transaminases hepáticas, confirmando uma relação entre este aumento e o medicamento. Em ensaios clínicos, as elevações das transaminases hepáticas ocorreram em qualquer momento durante o tratamento, embora a maioria tenha ocorrido nos primeiros 12 meses. Os níveis de ALT voltaram ao normal aproximadamente 2 meses após interromper o tratamento com Gilenya. Em um pequeno número de pacientes (N = 10 na dose de 1,25 mg, N = 2 na dose de 0,5 mg), que experimentaram elevações de ALT ≥5 vezes o limite superior da faixa normal e que continuaram a terapia com Gilenya, valores de ALT voltou ao normal em aproximadamente 5 meses (ver também secção 4.4 Função hepática).
Doenças do sistema nervoso
Em estudos clínicos, eventos raros envolvendo o sistema nervoso, incluindo acidente vascular cerebral isquêmico e hemorrágico e distúrbios neurológicos atípicos, como, por exemplo, eventos semelhantes a encefalomielite disseminada aguda (EAD).
Patologias vasculares
Casos raros de doença arterial periférica ocorreram em pacientes tratados com fingolimod nas doses mais altas (1,25 mg).
Sistema respiratório
Durante o tratamento com Gilenya, observaram-se ligeiras diminuições dose-dependentes no volume expiratório forçado (FEV1) e na capacidade de difusão do monóxido de carbono (Dlco), diminuições que ocorreram no primeiro mês e permaneceram estáveis ao longo do tratamento. No mês 24, a redução percentual da linha de base no VEF1 previsto foi de 2,7% para fingolimode 0,5 mg e 1,2% para placebo, uma diferença que foi resolvida após a interrupção do tratamento. As reduções de Dlco no mês 24 foram de 3,3% para fingolimode 0,5 mg e 2,7% para o placebo.
Linfomas
Foram notificados casos de vários tipos de linfoma em ensaios clínicos e na experiência pós-comercialização, incluindo um caso fatal de linfoma de células B positivo para o vírus Epstein-Barr (EBV). A incidência de casos de linfoma (células B e células T ) foi mais alto em estudos clínicos do que o esperado na população em geral.
Síndrome hemofagocítica
Foram relatados casos muito raros de síndrome hemofagocítica (Síndrome hemofagocítica, HPS) com resultado fatal em pacientes tratados com fingolimod no contexto de uma "infecção". HPS é uma condição rara que foi descrita em associação com infecções, imunossupressão e uma variedade de doenças autoimunes.
Notificação de suspeitas de reações adversas
A notificação de suspeitas de reações adversas ocorridas após a autorização do medicamento é importante porque permite a monitorização contínua da relação benefício / risco do medicamento. Pede-se aos profissionais de saúde que notifiquem quaisquer suspeitas de reações adversas através do sistema nacional de notificação. No "Anexo V .
04.9 Overdose
Doses únicas até 80 vezes a dose recomendada (0,5 mg) foram bem toleradas em voluntários saudáveis. Na dose de 40 mg, 5 dos 6 indivíduos relataram aperto no peito fraco ou mal-estar clinicamente relacionado à reatividade das vias aéreas.
O fingolimod pode induzir bradicardia no início do tratamento. A diminuição da frequência cardíaca geralmente ocorre dentro de uma hora após a primeira dose e é máxima nas primeiras 6 horas. O efeito cronotrópico negativo de Gilenya persiste para além de 6 horas e diminui progressivamente ao longo dos dias de tratamento seguintes (ver secção 4.4 para mais detalhes). Têm havido notificações de desaceleração da condução atrioventricular, com notificações isoladas de bloqueio atrioventricular. Resolução completa, transitória e espontânea (ver seções 4.4 e 4.8).
Se a sobredosagem coincidir com a primeira exposição a Gilenya, é importante que o doente tenha monitorização electrocardiográfica contínua (em tempo real) com medição da frequência cardíaca e tensão arterial de hora a hora, pelo menos durante as primeiras 6 horas (ver secção 4.4).
Monitoramento adicional também é necessário (pelo menos até a manhã seguinte e em qualquer caso até que os sintomas sejam resolvidos) se, após 6 horas da administração da primeira dose, a freqüência cardíaca for
O fingolimod não é eliminado por diálise ou plasmaférese.
05.0 PROPRIEDADES FARMACOLÓGICAS
05.1 Propriedades farmacodinâmicas
Grupo farmacoterapêutico: imunossupressores seletivos.
Código ATC: L04AA27.
Mecanismo de ação
O fingolimod é um modulador do receptor de esfingosina-1-fosfato (S1P). Por meio da esfingosina quinase, fingolimod é transformado no metabólito ativo fingolimod fosfato que se liga, em baixas concentrações nanomolares, ao receptor S1P1 localizado na superfície dos linfócitos e atravessa facilmente a barreira hematoencefálica para se ligar ao receptor no sistema nervoso central sistema S1P1 colocado nas células do sistema nervoso central. O fosfato de fingolimod, atuando como um antagonista funcional dos receptores S1P expressos nos linfócitos, inibe a capacidade dos linfócitos de escaparem dos linfonodos, resultando na redistribuição em vez da destruição dos linfócitos. Essa redistribuição reduz a infiltração de linfócitos patogênicos no sistema nervoso central, onde estão envolvidos na inflamação do nervo e dano ao tecido. Estudos e experimentos com animais em vitro indicam que fingolimod também pode atuar interagindo com os receptores S1P expressos nas células do sistema nervoso central.
Efeitos farmacodinâmicos
Dentro de 4-6 horas após a primeira administração de 0,5 mg de fingolimode, o número de linfócitos no sangue periférico é reduzido para aproximadamente 75% do valor basal. Continuando com a administração diária, o número de linfócitos continua diminuindo por duas semanas, atingindo um valor mínimo de cerca de 500 células / microlitro, ou cerca de 30% do valor basal. 18% dos pacientes atingiram um valor mínimo abaixo de 200 células / microlitro pelo menos uma vez. Com o tratamento diário contínuo, o número de linfócitos permanece baixo. A maioria dos linfócitos T e B migra regularmente através dos órgãos linfóides: o fingolimode atua principalmente nessas células. Cerca de 15-20% dos linfócitos T têm um fenótipo TEM (efetor de memória): essas células são importantes para a vigilância imunológica periférica. Como esse tipo de linfócitos geralmente não migra para os órgãos linfoides, o fingolimod não atua nessas células. O aumento do número de linfócitos periféricos é evidente nos dias que se seguem à descontinuação do tratamento com fingolimod; as contagens de linfócitos geralmente voltam ao normal dentro de um a dois meses. A administração crônica de fingolimod resulta em uma ligeira diminuição no número de neutrófilos igual a aproximadamente 80% do valor basal. O fingolimode não atua nos monócitos.
O fingolimod causa uma redução transitória da frequência cardíaca e diminuição da condução atrioventricular no início do tratamento (ver secções 4.4 e 4.8) 70% do efeito cronotrópico negativo. Com as administrações subsequentes, a freqüência cardíaca retorna à linha de base dentro de um mês. A redução da freqüência cardíaca induzida por fingolimod pode ser revertida pela administração parenteral de atropina ou isoprenalina. O salmeterol inalado também demonstrou ter um efeito cronotrópico positivo modesto. Ao iniciar o tratamento com fingolimode, há um aumento nas contrações atriais prematuras, mas não há aumento na taxa de fibrilação / flutter atrial ou arritmias ventriculares ou ectopia. O tratamento com fingolimode não resulta em diminuição do débito cardíaco e não afeta as respostas simpatomiméticas do coração, incluindo a variação da freqüência cardíaca diurna e a resposta ao esforço.
O tratamento com fingolimode, em doses únicas ou repetidas de 0,5 mg e 1,25 mg por duas semanas, não resulta em um aumento perceptível na resistência das vias aéreas medida como VEF1 e Fluxo Expiratório Forçado (FEF) 25-75. No entanto, com doses únicas de fingolimode ≥5 mg (10 vezes a dose recomendada), ocorre um aumento dependente da dose na resistência das vias respiratórias. O tratamento com doses repetidas de fingolimode de 0,5 mg, 1,25 mg ou 5 mg não resulta em oxigenação prejudicada ou dessaturação de oxigênio sob exercício ou um aumento na resposta das vias aéreas à metacolina. Os indivíduos tratados com fingolimode respondem com broncodilatação normal aos beta-agonistas inalados.
Eficácia clínica e segurança
A eficácia de Gilenya foi demonstrada em dois estudos que avaliaram a administração uma vez por dia de fingolimode 0,5 mg e 1,25 mg em pacientes com esclerose múltipla recorrente-remitente (EMRR). Ambos os estudos incluíram pacientes que tiveram ≥ 2 recidivas nos 2 anos anteriores ou ≥1 recaídas no ano anterior. A pontuação na Escala Expandida do Status de Incapacidade (EDSS) foi de 0-5,5. Um terceiro estudo conduzido na mesma população de pacientes foi concluído após o registro de Gilenya.
No estudo randomizado duplo-cego controlado com placebo, de 2 anos, D2301 (FREEDOMS), 1.272 pacientes foram incluídos (n = 425 tratados com fingolimode 0,5 mg, 429 com fingolimode 1,25 mg, 418 com placebo). Os valores medianos das características basais foram: idade 37 anos, duração da doença 6,7 anos, pontuação EDSS de 2,0. Os resultados são apresentados na Tabela 1. Não houve diferenças significativas entre as doses de 0,5 mg e 1,25 mg para todos os parâmetros.
Tabela 1: Estudo D2301 (LIBERDADES): Principais resultados
† Progressão da deficiência definida como aumento de 1 ponto em EDSS confirmado em 3 meses
** p
Todos os desfechos clínicos foram avaliados por análise intenção de tratar. As análises relacionadas aos dados de MRI usaram conjuntos de dados avaliáveis.
Pacientes que completaram a fase essencial do estudo FREEDOMS de 24 meses foram capazes de entrar na fase de extensão cega da dose (D2301E1) e receber fingolimod. Um total de 920 pacientes entraram (n = 331 continuaram com a dose de 0,5 mg, 289 com a dose de 1,25 mg, 155 mudaram de placebo para 0,5 mg e 145 de placebo para 1,25 mg). Após 12 meses (mês 36), 856 pacientes (93%) ainda estavam inscritos. Entre o mês 24 e o mês 36, a taxa de recaída anual (ARR) para pacientes que recebem fingolimode 0,5 mg na fase essencial do estudo e que continuou na mesma dose (0,5 mg) foi de 0,17 (0,21 na fase essencial de estudo). A taxa de recaída anual para pacientes que mudaram de placebo para fingolimode 0,5 mg foi de 0,22 (0,42 na fase essencial de estudo).
Resultados semelhantes foram obtidos em um estudo de Fase III, 2 anos, randomizado, duplo-cego controlado por placebo (D2309; FREEDOMS 2) conduzido em 1.083 pacientes com esclerose múltipla recorrente-remitente (n = 358 tratados com fingolimod 0, 5 mg, 370 com fingolimode 1,25 mg, 355 com placebo). Os valores medianos das características basais foram: idade 41 anos, duração da doença 8,9 anos, pontuação EDSS de 2,5.
Tabela 2: Estudo D2309 (LIBERDADES 2): Principais resultados
† Progressão da deficiência definida como aumento de 1 ponto em EDSS confirmado em 3 meses
** p
Todos os desfechos clínicos foram avaliados por análise intenção de tratar. As análises relacionadas aos dados de MRI usaram conjuntos de dados avaliáveis.
No estudo D2302 (TRANSFORMAS), fase III, com duração de 1 ano, randomizado, duplo-cego controlado e manequim duplo versus droga ativa (interferon beta-1α) 1.280 pacientes foram incluídos (n = 429 tratados com fingolimode 0,5 mg, 420 com fingolimode 1,25 mg, 431 com injeção intramuscular de interferon beta-1α em uma dose de 30 microgramas uma vez por semana). Os valores medianos das características basais foram: idade 36 anos, duração da doença 5,9 anos, pontuação EDSS de 2,0. Os resultados do estudo são apresentados na Tabela 3. Não houve diferença significativa entre as doses de 0,5 mg e 1,25 mg em relação aos pontos finais do estudo.
Tabela 3: Estudo D2302 (TRANSFORMAS): Principais resultados
† Progressão da deficiência definida como aumento de 1 ponto em EDSS confirmado em 3 meses
** p
Todos os desfechos clínicos foram avaliados por análise intenção de tratar. As análises relacionadas aos dados de MRI usaram conjuntos de dados avaliáveis.
Pacientes que completaram a fase essencial do estudo TRANSFORMS de 12 meses foram capazes de entrar na fase de extensão cega da dose (D2302E1) e receber fingolimode. Um total de 1.030 pacientes entraram, no entanto, 3 deles não receberam tratamento (n = 356 continuaram na dose de 0,5 mg, 330 na dose de 1,25 mg, 167 mudaram de interferon beta-1α para 0, 5 mg e 174 de interferon beta -1α a 1,25 mg). Após 12 meses (mês 24), 882 pacientes (86%) ainda estavam inscritos. Entre os meses 12 e 24, a taxa de recaída anual (ARR) para pacientes que recebem fingolimode 0,5 mg na fase essencial do estudo e que continuou na mesma dose (0,5 mg) foi de 0,20 (0,19 na fase essencial de estudo). A taxa de recaída anual para pacientes que mudaram de interferon beta-1α para fingolimode 0,5 mg foi de 0,33 (0,48 na fase essencial de estudo).
Os resultados combinados dos estudos D2301 e D2302 mostraram uma redução consistente e estatisticamente significativa do controle na taxa de recaída anual em subgrupos definidos por gênero, idade, terapia de MS anterior, atividade da doença ou deficiência no início do estudo.
Uma análise mais aprofundada dos resultados dos ensaios clínicos demonstra efeitos significativos do tratamento em subgrupos de pacientes com esclerose múltipla recorrente-remitente altamente ativa.
A Agência Europeia de Medicamentos diferiu a obrigação de apresentação dos resultados dos estudos com Gilenya em um ou mais subgrupos da população pediátrica na esclerose múltipla (ver secção 4.2 para informação sobre utilização pediátrica).
05.2 "Propriedades farmacocinéticas
Os dados farmacocinéticos foram obtidos em voluntários saudáveis, pacientes com transplante renal e pacientes com esclerose múltipla.
O metabólito farmacologicamente ativo responsável pela eficácia é o fosfato de fingolimod.
Absorção
A absorção de fingolimod ocorre lentamente (Tmax de 12-16 horas) e é extensa (≥85%). A biodisponibilidade absoluta aparente após a administração oral é de 93% (intervalo de confiança: 79-111%). curso estável são alcançados dentro de 1 a 2 meses após a administração de doses únicas diárias de fingolimod e níveis de allo curso estável eles são cerca de 10 vezes maiores do que aqueles observados com a dose inicial.
A ingestão de alimentos não altera a concentração de pico (Cmax) ou o valor de exposição sistêmica (AUC) do fingolimod. A Cmax do fosfato de fingolimod aumentou ligeiramente 34% enquanto a AUC se manteve inalterada.Portanto Gilenya pode ser tomado com o estômago cheio ou vazio (ver secção 4.2).
Distribuição
O fingolimode se distribui rapidamente nas hemácias e está presente em 86% das células sanguíneas. O fosfato de fingolimode tem uma distribuição 17% menor nas hemácias. A ligação do fingolimode e do fosfato de fingolimode às proteínas plasmáticas é alta (> 99%).
O fingolimod é amplamente distribuído nos tecidos, com um volume de distribuição de aproximadamente 1.200 ± 260 litros.
Biotransformação
Em humanos, fingolimode é metabolizado por fosforilação estereosseletiva reversível com formação do enantiômero (S) farmacologicamente ativo de fosfato de fingolimode. O fingolimod é eliminado por biotransformação oxidativa, catalisada principalmente pelo CYP4F2 e possivelmente outras isoenzimas, e subsequente degradação em metabólitos inativos, semelhante ao dos ácidos graxos. A formação de análogos de ceramida apolares farmacologicamente inativos de fingolimod também foi observada. A principal enzima envolvida no metabolismo do fingolimod foi parcialmente identificada e pode ser CYP4F2 ou CYP3A4.
Após uma única administração oral de fingolimode [14C], os principais componentes relacionados ao fingolimode, detectados no sangue por sua contribuição para a AUC até 34 dias após a administração do total de componentes marcados radioactivamente, são o próprio fingolimode (23%), o fosfato de fingolimode ( 10%) e alguns metabólitos inativos (metabólito de ácido carboxílico M3 (8%), metabólito de ceramida M29 (9%) e metabólito de ceramida M30 (7%)).
Eliminação
A depuração sanguínea de fingolimode é de 6,3 ± 2,3 L / he a meia-vida de eliminação terminal média (t1 / 2) é de 6-9 dias. Os níveis sanguíneos de fingolimode e fosfato de fingolimode diminuem em paralelo na fase terminal, resultando em metade semelhante -vive para ambas as moléculas.
Após administração oral, aproximadamente 81% da dose é excretada lentamente na urina como metabólitos inativos. Fingolimode e fosfato de fingolimode não são excretados inalterados na urina, mas estão presentes como componentes principais nas fezes, com quantidades cada um representando menos de 2,5% da dose Após 34 dias, a recuperação da dose administrada é de 89%.
Linearidade
As concentrações de fingolimode e fosfato de fingolimode aumentam de forma aparentemente proporcional à dose após a administração repetida de doses únicas diárias de 0,5 mg ou 1,25 mg.
Características em populações específicas
A farmacocinética do fingolimode e do fosfato de fingolimode não é diferenciada entre homens e mulheres, em pacientes de diferentes origens étnicas ou em pacientes com insuficiência renal leve a grave.
Em indivíduos com insuficiência hepática ligeira, moderada ou grave (classes A, B e C de Child-Pugh), não foi observada alteração na Cmax do fingolimode, enquanto a AUC do fingolimode aumentou 12%, 44% e 103%. Em doentes com insuficiência hepática grave ( Child-Pugh classe C), Cmax de fosfato de fingolimode diminuiu 22% e a AUC não foi substancialmente alterada. A farmacocinética do fosfato de fingolimod não foi avaliada em pacientes com insuficiência hepática leve a moderada. A meia-vida de eliminação aparente de fingolimod não foi alterada em indivíduos com insuficiência hepática leve, enquanto aumentou em aproximadamente 50% em pacientes com insuficiência hepática moderada ou grave.
O fingolimod não deve ser utilizado em doentes com compromisso hepático grave (Child-Pugh classe C) (ver secção 4.3). A terapêutica com fingolimod deve ser iniciada com precaução em doentes com compromisso hepático ligeiro a moderado (ver secção 4.2).
A experiência clínica e os dados farmacocinéticos em doentes com idade superior a 65 anos são limitados.Gilenya deve ser utilizado com precaução em doentes com idade igual ou superior a 65 anos (ver secção 4.2).
População pediátrica
Os dados de um estudo de transplante renal incluindo 7 crianças com mais de 11 anos de idade são limitados (estudo FTY720A0115). A comparação destes dados com os de voluntários adultos saudáveis é de pouca relevância e não podem ser tiradas conclusões significativas sobre as propriedades farmacocinéticas do fingolimod em crianças.
05.3 Dados de segurança pré-clínica
O perfil de segurança pré-clínico do fingolimod foi avaliado em camundongos, ratos, cães e macacos.Os principais órgãos-alvo foram o sistema linfóide (linfopenia e atrofia linfóide), os pulmões (ganho de peso, hipertrofia do músculo liso na junção bronquioloalveolar) e, em várias espécies, o coração (efeito cronotrópico negativo, aumento da pressão arterial, alterações perivasculares e miocárdicas degeneração); em um estudo de 2 anos, fingolimod foi ativo nos vasos sanguíneos (vasculopatia) apenas em ratos em doses de 0,15 mg / kg e superiores, equivalente a aproximadamente 4 vezes a exposição sistêmica humana (AUC) em uma dose diária de 0,5 mg.
Nenhuma evidência de carcinogenicidade foi observada em um estudo de 2 anos em ratos com doses orais de fingolimode até a dose máxima tolerada de 2,5 mg / kg, o que representa uma margem de aproximadamente 50 vezes a exposição sistêmica humana (AUC) em uma dose de 0,5 mg. No entanto, em um estudo de 2 anos em camundongos, uma maior incidência de linfoma maligno foi observada com doses de 0,25 mg / kg e superiores, equivalente a aproximadamente 6 vezes a exposição humana sistêmica (AUC) em uma dose diária de 0,5 mg.
Em estudos com animais, o fingolimod não foi considerado mutagénico ou clastogénico.
O fingolimod não teve efeito na contagem / motilidade de espermatozoides ou fertilidade de ratos machos e fêmeas até a dose máxima testada (10 mg / kg), o que representa uma margem de aproximadamente 150 vezes a exposição sistêmica humana (AUC) em uma dose diária de 0,5 mg.
O fingolimod demonstrou ser teratogênico em ratos quando administrado em doses de 0,1 mg / kg ou mais. As malformações viscerais fetais mais comuns incluem tronco arterial persistente e defeito do septo ventricular. O potencial teratogénico em coelhos não pode ser totalmente avaliado, no entanto, foi observado um aumento da mortalidade embriofetal com doses de 1,5 mg / kg e superiores, e diminuição de fetos viáveis, bem como retardo do crescimento fetal com doses de 5 mg / kg. Kg.
Em ratos, a sobrevivência da geração F1 de filhotes diminuiu no período pós-parto inicial com doses que não causaram toxicidade materna. No entanto, a geração F1 não foi afetada pelo tratamento com fingolimod no que diz respeito ao peso corporal, desenvolvimento, comportamento e fertilidade.
O fingolimod foi excretado no leite de animais lactantes tratados.O fingolimod e os seus metabolitos atravessaram a barreira placentária em coelhas grávidas.
Avaliação de Risco Ambiental (Avaliação de Risco Ambiental, ERA)
Nenhum risco ambiental é antecipado com o uso de Gilenya por pacientes com esclerose múltipla recorrente.
06.0 INFORMAÇÕES FARMACÊUTICAS
06.1 Excipientes
Conteúdo da cápsula:
Estearato de magnesio
Manitol
Concha da cápsula:
Óxido de ferro amarelo (E172)
Dióxido de titânio (E171)
Geléia
Tinta:
Laca (E904)
Álcool desidratado
Álcool isopropílico
Álcool butilico
Propileno glicol
Água purificada
Solução concentrada de amônia
Hidróxido de potássio
Óxido de ferro preto (E172)
Óxido de ferro amarelo (E172)
Dióxido de titânio (E171)
Dimeticona
06.2 Incompatibilidade
Não é relevante.
06.3 Período de validade
2 anos.
06.4 Precauções especiais de armazenamento
Não armazene acima de 25 ° C.
Conservar na embalagem original para proteger o medicamento da umidade.
06.5 Natureza da embalagem primária e conteúdo da embalagem
Embalagens contendo 7, 28 ou 98 cápsulas ou embalagens múltiplas contendo 84 (3 embalagens de 28) em blisters de PVC / PVDC / alumínio.
Embalagens contendo 7 x 1 cápsulas em blisters destacáveis para dose unitária em PVC / PVDC / alumínio.
Nem todos os tamanhos de embalagem podem ser comercializados.
06.6 Instruções de uso e manuseio
Sem instruções especiais.
07.0 TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
Novartis Europharm Limited
Wimblehurst Road
Horsham
West Sussex, RH12 5AB
Reino Unido
08.0 NÚMERO DE AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
EU / 1/11/677 / 001-006
040949012
040949024
040949036
040949048
040949051
09.0 DATA DA PRIMEIRA AUTORIZAÇÃO OU RENOVAÇÃO DA AUTORIZAÇÃO
17.03.2011
10.0 DATA DE REVISÃO DO TEXTO
Junho de 2014












.jpg)